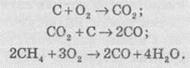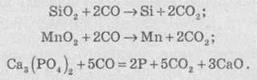|
Чугун
и сталь Самые распространенные
сплавы - чугун и сталь. Оба эти сплавы являются сплавами на основе железа.
Главное отличие между ними - это содержание углерода. Если содержание углерода превышает 4
%, то такой сплав называют чугуном. Если же содержание углерода меньше 4 %, то такой
сплав называют сталью. Содержание углерода в этих сплавах существенно влияет на их
физические свойства. Если чугун является твердым и хрупким, то, в отличие от него,
сталь представляет собой более мягкий и пластичный сплав. Кроме того, в состав стали
добавляют еще некоторые другие металлы для добывания стали с необходимыми характеристиками.
Так, добавление к стали марганца повышает ее износостойкость, что позволяет
использовать ее для изготовления железнодорожных рельсов. А добавление хрома увеличивает
устойчивость к коррозии; такую сталь называют іржостійкою. Соответственно,
содержание в этих сплавах определенных добавок определяет область их применения в народном
хозяйстве. Еще
в древние времена, несколько тысячелетий назад, металлурги умели добывать непосредственно
из руды (железо оксида) мягкий сорт стали. Для этого в небольших печах (горнах) заключали
слоями железную руду и древесный уголь. Температуру, необходимую для преобразования
руды в металл (восстановления железа), получали с помощью дутья. В конце
процесса, длившегося несколько часов, выходил металл в твердом состоянии, в виде
губчатой массы. Его извлекали из горнов и ковали. В XVIII в. началась
промышленная революция. Под влиянием растущего спроса на металл начали строить
более объемные горны и применять более интенсивное дутье. Изменение технологии
привела к нежелательным результатам: в горнах, кроме твердой стали, выходил
побочный продукт - жидкий чугун. В отличие от стали, он нековкий и
непригоден для применения. Позже был разработан относительно простой способ
переработки чугуна в сталь: через жидкий чугун продували воздух. При этом
углерод выгорал, и сплав приобретает пластичности. С открытием способа переработки
чугуна в сталь начали строить большие печи и всю превращать руду в чугун. Как
сырье для производства чугуна используют железную руду, состоящую из
оксидов Железа, чаще всего Fe2O3. Она содержит также пустую породу, к
состав которой входят соединения Кремния (SiO2), Марганца
(МnO2),
Алюминия (Аl2O3), Фосфора (Са3(РO4)2),
Серы (FeS2, CaSO4) и
др. Перед
плавкой руду обогащают - удаляют из нее определенную часть пустой породы,
затем измельчают крупные куски руды до необходимых (оптимальных) размеров, а
пилувату руду спекают с углем подвергают агломерации. В
доменной печи протекает огромное число реакций, которые разделяют на несколько
групп. 1-я
группа реакций. Горения
кокса и образование восстановителя - карбон(II) оксида. Сегодня в домны, кроме
воздух, поступает природный газ, который интенсифицирует процесс плавки и позволяет
уменьшать расход дорогостоящего кокса:
2-га
группа реакций. Восстановление
ферум(ІІІ) оксида карбон(II) оксидом протекает тремя последовательными стадиями:
3-я
группа реакций. Восстановление
примесей. Благодаря этой группе ре акций много элементов пустой породы
переходят в чугун:
Часть
Серы из природных соединений переходит в чугун в виде соединения FeS, а часть - в
сернистый газ SО2, который выходит из
доменной печи в смеси с другими газами, а затем улавливается. 4-и
группа реакций. Образование
чугуна чаще всего описывают с помощью уравнения реакции между железом и коксом,
а также между железом и угарным газом:
5-и
группа реакций. Образование
шлака происходит следующим образом. Флюсы под воздействием высоких температур разлагаются
с образованием реакционно-способных основных оксидов СаО и MgO. Они реагируют с
теми компонентами пустой породы, которые имеют кислотные или амфотерные
свойства, например SiО2 и Аl2O3. Образуемые
в процессе плавки силикаты, алюмосиликаты, алюминаты, некоторые сульфиды образуют
побочный продукт доменного производства - шлак. Он отмечается небольшой
плотностью и поэтому накапливается на поверхности чугуна, предотвращая его окисление.
|
|