Часть II.
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Раздел 9. ПОДГРУППА
КИСЛОРОДА
§
9.5. Оксид серы(ИV).
Сульфитная кислота
Оксид серы(ИV). Оксид серы(ИV), или сернистый газ, при обычных условиях
- бесцветный газ с резким, удушливым запахом. Во время охлаждения до - 10°С
сжижается в бесцветную жидкость. В жидком состоянии его хранят в стальных
баллонах.
В
лабораторных условиях оксид серы(ИV) получают взаимодействием гидросульфита натрия с серной
кислотой:
2Na2HSO3
+ H2SO4
= Na2SO4
+ 2SO2
↑ + 2Н2O,
а также нагреванием меди с
концентрированной серной кислотой:
Cu + 2H2SO4
= CuSВ4 + SO2
↑ + 2Н2О.
Оксид серы(IV) образуется также
во время сжигания серы.
В промышленных условиях SO2 добывают во время выжигания
пирита FeS2 или сернистых руд цветных
металлов (цинковой обманки ZnS,
свинцового блеска PbS и т.д.).
Оксид серы(ИV)
SO2,
образуется при этих условиях используют в основном для извлечения оксида
серы(VИ)
SO3 и сульфатной кислоты H2SO4 (см. § 9.6). Структурная формула
молекулы SO2:
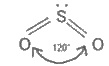
Как видим, в образовании связей в
молекуле SO2 берут
участие четыре электроны серы и четыре электрона от двух атомов кислорода.
Взаимное отталкивание связывающих электронных пар и неподеленной электронной пары
атома серы придает молекуле угловой формы.
При наличии катализатора во время
нагрева SO2 присоединяет кислород воздуха и
образуется SO3:
+4
+6
2SO2 + O2 ⇆ 2SO3.
В этой реакции сульфур меняет степень
окисления от +4 до +6, следовательно, для SO2 характерны восстановительные свойства.
Оксид серы(ИV) проявляет все свойства кислотных
оксидов.
Сульфитная кислота. Оксид серы(ИV) хорошо растворим в воде (в 1 объеме
воды при 20°С растворяется 40 объемов SO2). При этом образуется сульфитная
кислота, которая существует только в водном растворе:
SO2 + Н2O
⇆ H2SO3.
span style='font-family:"Verdana","sans-serif"'>Реакция
сочетание SO2 с
водой обратима. В водном растворе оксид серы (IV) и сульфитная кислота
находятся в состоянии химического равновесия, которую можно смещать. При связывании H2SO3 щелочью (нейтрализация кислоты)
реакция идет в сторону образования сульфитной кислоты; при удалении SO2 (продувания через раствор азота или
нагрева) - в сторону образования исходных веществ. В растворе сульфитной кислоты
всегда содержится оксид серы(ИV), который предоставляет ему резкого запаха.
Сульфитная кислота имеет все
свойства кислот. В растворе H2SO3 диссоциирует
ступенчато:
H2SO3
⇆ Н+ + HSO3
;
HSO-3
⇆Н+ + SO2-3.
Как двохосновна кислота, она образует
два ряда солей - сульфиты и гідросульфіти. Сульфиты образуются при полной
нейтрализации кислоты щелочью:
H2SO3 + 2NaOH = Na2SO3 + 2Н2О.
Гідросульфіти образуются при
недостаточном количестве щелочи (по сравнению с количеством, необходимым для полного
нейтрализации кислоты):
H2SO3 + NaOH = NaHSO3 + Н2О.
Как и оксид серы(ИV), сульфитная кислота и ее соли
сильными восстановителями. При этом степень окисления серы возрастает. Так, H2SO3 легко окисляется
к
серной кислоты даже кислородом
воздух:
2H2SO3 + O2 = 2H2SO4.
Поэтому растворы сульфитной кислоты,
долго хранились, всегда содержат сульфатную кислоту.
Еще легче происходит окисления
сульфитной кислоты бромом и перманганатом калия:
+4
0
+6
-1
H2SO3
+ Вr2 + Н2O = H2SO4
+ 2НВк;
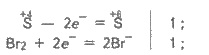
5H2SO3
+ 2КМnO4 = 2H2SO4
+ 2MnSO4
+ K2SO4
+ 2Н2O;
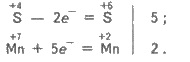
Оксид серы(ИV) и сульфитная кислота обесцвечивают
много красителей, образуя с ними бесцветные соединения. Последние могут вновь
разлагаться при нагревании или при освещении, вследствие чего окраска
восстанавливается. Итак, отбеливающее действие SO2 и H2SO3 отличается от отбеливающей действия
хлора. Конечно оксидом серы(ИV) отбеливают шерсть, шелк и солому (хлорной водой эти
материалы разрушаются).
Оксид серы(ИV) убивает многие микроорганизмы.
Поэтому для уничтожения плесневых грибов им окуривают сырые подвалы, погреба, винные
бочки и т.д. Используют его также во время транспортировки и хранения
фруктов и ягод. Много оксида серы(ИV) нужно для добывания серной
кислоты.
Широко применяется раствор
гидросульфита кальция Ca(HSO3)2 (сульфитный
митель), которым обрабатывают волокна древесины и бумажную массу.