|
Электронная
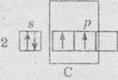
строение атомов Углерода и Кремния схематично показана ниже:
В
невозбужденном состоянии атомы Углерода и Кремния двухвалентные, потому что на внешнем
уровне находится 2 неспаренных электрона:
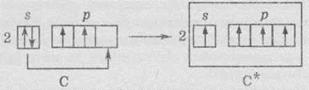
При
возбуждении атома происходит розпаровування электронной пары, которая находится на
2в-подуровне. При этом Карбон и Кремний проявляют четырехвалентное состояние. На
следующей схеме изображен электронный переход при образовании чотиривалентного
состояния для атома Углерода; процессы, которые происходят в электронной оболочке атома
Кремния, аналогичные:
На
отличие от элементов, рассмотренных ранее (галогены, халькогени и пніктогени),
для атомов Углерода и Кремния нехарактерные электронные переходы с участием
вакантной d-подуровня, поэтому
высшая валентность этих атомов равна 4. Оба
элементы могут проявлять степени окисления -4, +2 и +4. Распространенность
атомов в природе Карбон
является достаточно распространенным, элементом на Земле. Его массовая доля составляет
около 0,023% по массе. В земной коре он встречается в виде соединений с
Гідрогеном - углеводородами, из которых состоит нефть (около 85% Углерода),
природный газ (около 70% Карбона), черное (около 90% Карбона) и бурый
уголь (около 70% Карбона) и горючие сланцы. Все эти соединения необходимы как
топливо для различных целей. Годовая добыча этих природных горючих веществ
составляет миллионы тонн. Атомы
Карбона входят также в состав многих минералов, таких как известняк, мел,
мрамор, основным компонентом которых является кальций карбонат (СаСО3);
доломит - CaMg(CО3)2;
престол - смесь Na2CO3 и NaHCВ3; магнезит - MgCВ3; смітсоніт - ZnCВ3; церусит - РbСO3; сидерит - FeCO3; родохрозит - МnСO3 и некоторые другие.
Кроме твердой поверхности земли, Карбон содержится также в атмосфере нашей планеты,
входя в состав углекислого газа
- СO2.
Около 2,3 span style='font-family:"Times New Roman","serif"'>∙
1012 тонн или 0,03% (по объему) атмосферы составляет углекислый
газ. В Мировом океане содержится около 4 ∙ 1013 тонн связанного
Углерода в виде карбонатов (СO32-)
и гидрогенкарбонатов (НСO3-). Карбон
является началом жизни на Земле. Начиная от простейшего одноклеточного организма
и заканчивая человеком, все живое на нашей планете содержит огромные количества Карбона.
Он необходим для жизни так же, как кирпич для строительства дома. Соединения
Карбона с некоторыми элементами (Гідрогеном Н, Оксисеном О, Азотом N и другими) изучает отдельная химическая
дисциплина - органическая химия. Карбон входит в состав белков, жиров, углеводов,
ДНК и большинства других биологически важных веществ. Силиция
- второй по распространенности элемент на Земле. Его содержание в земной коре составляет
29,5% по массе. Если Карбон является важнейшим элементом для живой материи, то
Кремний является основным компонентом неживой материи. Соединения, в состав которых входит
атом Кремния, составляют 74% от массы Земли. Самым распространенным
минералом, в состав которого входит атом Кремния, является кварц (или кремнезем) SiO2, что встречается в виде простого
песка. Из других минералов стоит выделить следующие: ортоклаз K2Al2Si6O16; каолин
Аи2O3
∙
2SiO2 ∙ 2Н2O; нефелін NaKO ∙ Аl2O3 ∙
2SiO2; циркон ZnSiO3; полуцит 3Cs2O ∙
2Аl2O3 ∙
9SiO2 ∙ Н2O. Силиция
в малых количествах необходим всем живым организмам. В организме человека Кремния
больше всего в ногтях и волосах, а в 1 грамме легочной ткани содержится 0,65 мг
Кремния.
|
|