Уравнение Менделеева - Клапейрона
Величины
p,
V и
T, которые определяют состояние газа, называют параметрами состояния. Уравнение, в состав которого одновременно входят все параметры, называется
уравнением состояния.
Давление
p газа зависит от значений
T и
V:
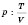
. Переход от пропорциональности к уравнению сначала было осуществлено с помощью коэффициента, который имел постоянное значение (константу) для данного газа, но имел различные значения для других газов (эта константа не была универсальной). Таким образом было получено уравнение состояния, названное уравнением Клапейрона:
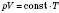
.
Коэффициент пропорциональности стал универсальным благодаря Дмитрию Менделееву, который предложил рассматривать различные газы в одинаковых количествах, поэтому уравнение стало называться уравнением Менделеева - Клапейрона.
Для 1 моль газа
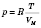
, или
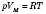
.
Величина
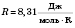
называется
универсальной (или
молярною)
газовой постоянной.
Для
n моль:
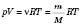
.