ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ
Валентность
При
образовании молекулы атомы не просто объединяются в какой-то беспорядочный клубок, а
связываются в определенной последовательности особыми химическими связями. Причем
каждый атом может образовать не бесконечное, а только определенное число таких связей. В
XIX веке ученые установили, что атомы разных элементов имеют разную способность
присоединять к себе другие атомы. Так, было отмечено, что атом Водорода может
присоединять только один атом другого химического элемента, атом Кислорода - два
атомы, Азота - три атома. Это свойство атомов было названо валентностью.
Валентность
- это число химических связей, которые атом может образовать с другим атомом.
Чтобы
показать, как атомы соединены в молекуле, часто используют структурные
формулы. В них показывают не только число атомов в молекуле, но и последовательность
их соединения.
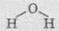
С
этой формулы видно, что в молекуле воды атом Кислорода соединен с двумя атомами
Водорода, причем атомы Водорода друг с другом не связаны. Каждый химический
связь в структурной формуле обозначен риской. Следовательно, атом Кислорода образуют
две связи - валентность Кислорода равна II (двовалентний), а атомы Водорода
образуют по одной связи - валентность Водорода равна И (одновалентний).
Рассмотрим
молекулу углекислого газа. Его структурная формула имеет такой вид:
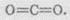
В
углекислом газе атомы Кислорода образуют по две связи с атомом Карбона
(такую связь называют двойным), а Карбон при этом образует четыре связи
(или две двойные связи). В этом соединении валентность Углерода равна IV.
В
различных элементов валентность может быть постоянной и переменной. Так, Водород
всегда одновалентний, а Кислород всегда двовалентний. Тем временем Сульфур может
быть двовалентним, четырехвалентен и шестивалентним.