ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ
Химическая символика.
Знаки химических элементов и химические формулы
К
химической символики относят символы химических элементов, химические формулы и
уравнения.
Символы
химических элементов состоят из одной или двух букв латинского алфавита с
числа тех, которые входят в состав латинского названия элемента. Большинство названий и,
соответственно, символов химических элементов сложились исторически и присваивались
первооткрывателями этих элементов. В последнее время в Периодической системе можно
встретить такие символы, как Unn. Подобные символы присваивают недавно открытым элементам,
для которых еще не утверждено название международным обществом фундаментальной и
прикладной химии (IUPAC). Для таких
элементов в названии и символе зашифровывают порядковый номер элемента на основании
латинского названия цифр. Например, элемент с порядковым номером 110 будет иметь
название унуннілій (ун - 1, нил - 0) и символ Uun, а элемент с
порядковым номером 118 - название унуноктий (ун - 1, окта - 8) и символ Uuo.
Химическими
символами обозначают: химический элемент; простое вещество с атомной или металлической
кристаллической решеткой (Al, Fe, С, Si); один атом
химического элемента.
Химические
формулы - это обозначение состава вещества с помощью знаков химических символов
и индексов.
Индекс
- это цифра, которую располагают справа внизу от символа химического элемента, он
указывает на число атомов этого элемента в молекуле вещества.
Различают
несколько видов химических формул (по рекомендациям IUPAC): эмпирические, молекулярные, электронные, структурные и дисплейные.
Молекулярные
формулы отражают качественный (из атомов каких элементов состоит вещество) и
количественный состав молекулы вещества. Например, запись СО2 означает,
что:
- в состав углекислого газа входят атомы
элементов Углерода и Кислорода;
- одна молекула углекислого газа состоит из
одного атома Углерода и двух атомов Кислорода.
Молекулярные
формулы можно применять только для веществ молекулярного строения. У веществ
ионной или атомной строения нельзя выделить отдельные молекулы, поэтому для них
применяют эмпирические формулы.
Эмпирические
формулы отражают качественный состав вещества и количественное соотношение между
атомами элементов в веществе (стехиометрическое соотношение).
Эмпирические
формулы применяют для веществ ионной или атомной строения, а также для отображения
результатов элементного анализа вещества.
Например,
натрий хлорид имеет ионное строение. Кристалл (надмолекула) натрий хлорида состоит
из большого количества положительно заряженных ионов Натрия и отрицательно заряженных
ионов Хлора. Причем в кристаллической решетке каждый ион Натрия окружен шестью ионами
Хлора, а каждый ион Хлора окружен шестью ионами Натрия, поэтому отдельную частицу,
которую можно назвать молекулой натрий хлорида, выделить невозможно. Однако в целом
в кристалле соотношение между ионами Натрия и Хлора равно 1:1. Следовательно,
надмолекулу натрий хлорида необходимо записать так: {Na+Cl-}m. Но
вместо этого удобнее пользоваться эмпирической формулой NaCl.
Эмпирические
формулы используют также для отражения элементного анализа. Например,
если по результатам анализа вещество состоит из атомов Углерода и Водорода
с соотношением 1:1, то для этого вещества можно записать эмпирическую формулу
СН. Однако без дополнительных данных сказать, что это за вещество, невозможно, ведь такая
эмпирическая формула справедлива для ацетилена (молекулярная формула С2Н2), бензену (молекулярная формула С6Н6),
циклодекапентаену (С10Н10) и т.д. Или же эмпирическая формула СН2
характерна для всех этиленовых углеводородов (например, этилен С2Н4
или бутен С4Н8), а также и для всех циклоалканів
(например, циклопропан С3Н6 или циклогексан С6Н12).
Электронные
формулы схематично отражают механизм образования химических связей в молекулах.
их записывают с помощью символов химических элементов и точек, которые обозначают
электроны внешнего электронного уровня. Например:

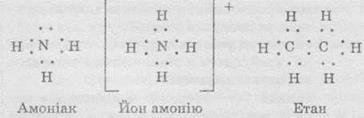
Структурные
формулы отражают порядок соединения атомов или групп атомов в молекулах.
Чаще всего структурные формулы используют для изображения молекул органических
веществ. Например:
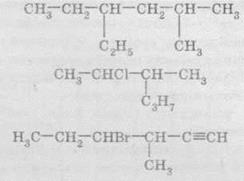
В
структурных формулах черточкой обозначают химическую связь, то есть одна общая
электронная пара. Структурные формулы используют только для отображения
соединения атомов, но не пространственного строения. Структурные формулы невозможно
использовать для изображения ионных соединений, поскольку в них отсутствуют общие
электронные пары. Структурными формулами пользуются для изображения
молекул или групп атомов, в которых атомы связаны ковалентними связями.
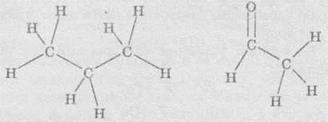
Дисплейные
формулы напоминают структурные формулы, однако в дисплейных формулах все связи
обозначают черточкой. Кроме того, часто в дисплейных формулах отражают валентные
углы между связями, поэтому с их помощью можно отображать пространственную
строение молекул.
Химические
уравнение - это условное изображение химической реакции с помощью химических
символов, формул и коэффициентов.
Например,
2NaOH + H2S → Na2S + 2H2О.
Коэффициенты
обозначают большой цифрой слева от формулы вещества. Коэффициент принадлежит
формуле только того вещества, рядом с которой он стоит. Коэффициент показывает
число отдельных атомов или молекул (или число молей вещества атомов или молекул),
которые участвуют в химической реакции.
При
записи уравнений химических реакций используют также следующие обозначения:
• символы →
или = разделяют исходные вещества и продукты реакции;
• символ 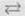 указывает на то, что исходные вещества
находятся в стали химического равновесия с продуктами реакции;
указывает на то, что исходные вещества
находятся в стали химического равновесия с продуктами реакции;
• символ ↑
- вещество выделяется в виде газа с конденсированной системы (смеси твердых
или жидких веществ);
• символ
↓
- вещество выпадает в осадок из раствора или смеси газов.
Иногда
еще указывают агрегатное состояние исходных веществ и продуктов реакции или
концентрацию раствора какой-либо исходного вещества: «тв» - твердое вещество, «г»
- жидкость, «г» - газ, «конц» - концентрированный раствор, «решения» - разведенный
раствор.
Уравнение
химических реакций разделяют на:
молекулярные
(для всех веществ записаны молекулярные или эмпирические формулы),
ионные
(записывают только ионы, которые участвуют в реакции),
электронные
и электронно-ионные уравнения напівреакцій (описывают процесс окисления или восстановления),
термохимические
(в молекулярных уравнениях указывают тепловой эффект реакции).
Например.
Молекулярные
уравнение реакции:
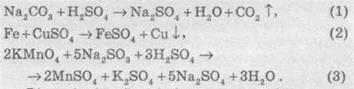
Соответствующие
им ионные уравнения реакций:
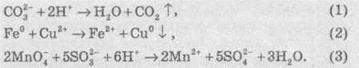
В
ионных и электронно-ионных уравнениях реакций указывают заряды ионов в растворах.
При записи заряда ионов сначала записывают величину заряда (арабской цифрой),
а потом знак заряда: 2-, 3+ и т.д.
Электронные
уравнение напівреакцій для уравнения (2):
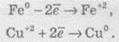
В
электронных уравнениях реакции указывают степень окисления атомов элементов. При
записи степени окисления сначала указывают знак, а затем значение степени
окисления: -2, +5 и т.д.
Электронно-ионные
уравнение напівреакцій для уравнения (3):
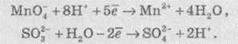
Также
часто используют термохимические уравнения реакций. Это обычные уравнения, в
которых указывают еще и тепловой эффект реакции, т.е. количество теплоты, которое
поглощается или выделяется в результате реакции. Примеры термохимических
уравнений реакций:
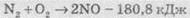 (эндотермический процесс), тепловой эффект реакции
Q = -180,8 кдж/ моль;
(эндотермический процесс), тепловой эффект реакции
Q = -180,8 кдж/ моль;
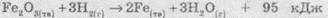 (экзотермический процесс), тепловой эффект реакции
Q = 95 кДж/ моль.
(экзотермический процесс), тепловой эффект реакции
Q = 95 кДж/ моль.
Уравнение
химических реакций отражают количественные (мольные) соотношение веществ,
вступают в реакцию и образуются в результате реакции. Поэтому иногда такие
уравнения и коэффициенты в них называют стехиометрическими уравнениями и
коэффициентами.