Часть И. ОБЩАЯ
ХИМИЯ
Раздел 1. ОСНОВНЫЕ
ПОНЯТИЯ И ЗАКОНЫ ХИМИИ
§
1.4. Относительная атомная масса
Современные методы исследования дают
возможность определить очень малые массы атомов с высокой точностью. Например,
масса атома водорода составляет 1,674 ∙ 10-27 кг, кислорода - 2,667 ∙ 10-26 кг, углерода - 1,993 ∙ 10-26 кг.
В химии традиционно используются
не абсолютные значения атомных масс, а относительные. В 1961 г. за единицу атомной
массы было принято атомную единицу массы (сокращенно а.е.м.). что представляет собой 1/12
часть массы атома изотопа углерода 2С.
Большинство химических элементов содержат
атомы с разной массой (см. изотопы, § 2.4). Поэтому относительной атомной массой Аr химического элемента называется
величина, равная отношению средней массы атома естественного изотопического
состав элемента к 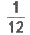 массе
атома углерода 12С.
массе
атома углерода 12С.
Относительные атомные массы1
элементов обозначают Аr
где индекс r
- начальная буква английского слова relative - “относительный”. Записи А(Н), А(O), А(С) означают: относительная атомная
масса водорода, относительная атомная масса кислорода, относительная атомная масса углерода.
Например:

Относительная атомная масса - одна из
основных характеристик химического элемента. Современные значения относительных атомных
масс приведены в периодической системе элементов Д. И. Менделеева.
1 Вместо термина "относительная
атомная масса” можно использовать термин “атомная масса”, возник исторически.