Часть 2 МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Раздел 7 ОСНОВЫ ТЕРМОДИНАМИКИ
7.4. Первый принцип термодинамики
Первый принцип термодинамики является
обобщающим законом сохранения и превращения энергии, сформулированным по
процессов, в которых участвует теплота.
Первый принцип термодинамики можно
сформулировать так: предоставленная системе теплота расходуется на увеличение ее
внутренней энергии, а также на работу против внешних сил.
Этим принципом было подведено
итог многочисленным экспериментам по созданию «вечного двигателя». Первый
проект такого двигателя известен еще в XIII ст. Однако уже в 1775 г. Французская
академия наук решила не принимать на рассмотрение проекты вечных двигателей. Первый
принцип утверждает: «перпетуум мобиле» (от лат, perpetuum mobile - вечно подвижной) первого рода невозможен. Под вечным
двигателем первого рода понимают такой двигатель, который, повторяя произвольное число
раз тот самый процесс, способный выполнить большую работу по сравнению с той
количеством энергии, которую он поглощает извне. Иначе говоря, «перпетуум мобиле»
первого рода - это такой двигатель, который сам бы порождал энергию. Если бы удалось
построить «перпетуум мобиле первого рода, человечеству не нужно было бы больше
беспокоиться о топливе, химическая энергия которого превращается в двигателях
внутреннего сгорания и в паровых машинах в энергию механическую, сооружать
плотины на реках для гідросилових установок и т.п.
Поэтому не удивительно, что было слишком много
попыток построить такой вечный двигатель. Однако это никому не удалось. Ответ на
вопрос «почему» дает первый принцип термодинамики. С философской точки зрения это
формулировка первого принципа термодинамики, а следовательно, и закона сохранения
энергии менее удовлетворительное, чем предыдущее, ибо оно оспаривающее его. Всякое утверждение,
представлено в отрицательной форме, имеет меньшую познавательную и научную ценность, чем
утверждение, поданное в утвердительной форме. В отрицательной форме закона
сохранения энергии кроется его конкретный, реальный смысл как универсального и
абсолютного закона природы. Самое главное в законе сохранения х. преобразования
энергии - это перетворюваність форм движения материи из одной в другую. Однако в
отрицательном формулировке закон сохранения энергии сводится к простому
утверждение о невозможности сконструировать машину, которая бы работала, не
тратя энергии. Этим ограниченным содержанием закона сохранения энергии в
указанной отрицательной форме пользовались махісти в своей борьбе против
материализма. Е. Мах, например, пытался доказать, что закон о невозможности
создание вечного двигателя первого рода тождественен закону причинности. Следовательно, он
не видел ничего нового в законе сохранения энергии, кроме простого констатирования
причинной связи между явлениями. Саму причинность Е. Мах понимал идеалистически,
как ограниченность нашего субъективного ожидания, а не закон природы. Рассмотрим
термодинамічну
систему, полная энергия
которой

где
Еп - потенциальная энергия системы; Ек - кинетическая энергия
системы; U - ее внутренняя энергия. Допустим,
что взаимодействия системы с внешней средой нет, тогда Еп = 0.
Если система неподвижна относительно внешних тел, то и Ек = 0.
Внутренняя энергия системы
состоит из кинетической и потенциальной энергий составляющих ее элементов:

Предположим, что в системе
происходит произвольный круговой процесс, когда система, претерпев изменений,
возвращается до самого начального состояния, как это схематически изображено на рис.
7.4. Изменится энергия системы в состоянии В после кругового процесса ВаСbВ? На основании многовекового
опыта, обобщенного в законе сохранения и превращения энергии, можно
ответить на этот вопрос так: внутренняя энергия системы в определенном состоянии есть
величиной постоянной и не зависит от того, как именно система пришла к этому
состояния.
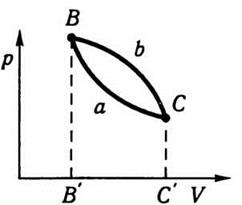
Рис. 7.4
Если система, переходя из состояния В
в состояние С, вследствие взаимодействия со средой получит энергию U1, а затем, возвращаясь к состоянию В,
отдаст среде энергию U2, то эти энергии равны друг другу: U1 = U2. Иначе получалось бы, если бы энергия
возникала из ничего или исчезала бесследно, это противоречило бы закону сохранения и
преобразования энергии. Отсюда следует важный вывод: внутренняя энергия
термодинамической системы является однозначной функцией состояния, т.е. каждому состоянию
соответствует определенное значение внутренней энергии. Понятно, что обратное
утверждение - каждому значению внутренней энергии соответствует определенное состояние -
совершенно неправильное, ибо определенному значению внутренней энергии могут соответствовать
разные состояния. Энергия является мерой движения. Движение является неотъемлемым свойством материи. Поэтому
увеличение или уменьшение энергии системы означает изменение в ней движения в количественном
и качественном отношениях. Изменение движения сопровождается изменением свойств
системы, ее физического состояния, который характеризуется определенными параметрами.
Предположение, что в том самом состоянии системы энергия может быть неодинаковой по
значением, равнозначно предположению, что движение не связан с материей, а является чем-то
внешним относительно нее. Однако это противоречит основам материалистической диалектики
о неразрывной связи материи и движения. Внутренняя энергия - однозначная функция
термодинамического состояния. Внутренняя энергия системы в состояниях В и С (см. рис. 7.4) определяется состояниями
системы и не зависит от того, как именно система перешла, например, из состояния В
в С (ВаС или ВbС). Следовательно, изменение внутренней энергии
системы при переходе из одного состояния в другое не зависит от способа (пути)
перехода; она зависит только от начального и конечного состояний. Это является еще
одним формулировке первого принципа термодинамики.
Перейдем к количественному
формулировка его. Рассмотрим термодинамическую систему, например, газ в цилиндре
с поршнем, который перемещается. В результате взаимодействия со средой энергия
переходит к системе или, наоборот, от системы к среде. Обмен энергией
может осуществляться только двумя способами: в результате работы или нагрева.
Эти два способа не исключают друг друга и могут действовать одновременно: например,
энергию газа можно увеличить одновременным сжатием и нагревом. Если тело не
получает извне никакой энергии, то работа, которую выполняет газ при своем
расширении, выполняется за счет его внутренней энергии. Эта энергия U складывается из кинетической энергии теплового движения молекул
и потенциальной энергии их взаимодействия.
Однако изменение внутренней энергии тела
при произвольном процессе, вообще говоря, не совпадает с выполненной работой, потому
тело может получать (или отдавать) энергию также через непосредственный переход
от других тел. При этом механическая работа не выполняется. Полученную таким образом
энергию называют количеством теплоты. Будем считать эту величину положительной, если
тело получает некоторое количество теплоты, и отрицательной, если оно отдает ее.
Пусть газа под поршнем предоставили
количество теплоты ΔQ = Q2 - Q1.
Вследствие расширения
газа поршень поднимется на высоту Δh. Если давление над поршнем остается постоянным (р = const), то работа, которую выполняет газ,
определяется формулой

Однако ΔQ
≠ ΔА,
поскольку часть подведенной к системе теплоты превращается во внутреннюю
энергию газа ДС/. Тогда справедливо такое равенство:

где
ΔQ - полученное количество теплоты; ΔА - работа, которая выполняется; ΔU - изменение внутренней энергии системы при переводе ее
во время нагревания из одного состояния в другое. Соотношение (7.9) является количественным
выражением закона сохранения энергии при тепловых процессах, то есть является первым
принципу термодинамики, которое можно сформулировать так: количество теплоты, предоставленная
системе, расходуется на приращение внутренней энергии и на выполнение системой
работы над внешними телами.
Вернемся к рис. 7.4. Пусть
система при нагревании переходит из состояния В в состояние С вначале путем ВаС, а
затем путем ВbС. Работа, которую выполнит система при
этом, будет определяться площадью, охваченной ВаС кривой, ординатами ВВ' и СС' и
осью объемов в первом случае, и площадью, охваченной кривой ВЬС, ординатами ВВ'
и СС' и осью объемов - во втором случае. Из рис. 7.4 видно, что эти площади разные:
при переходе из состояния В в состояние С путем ВаС система выполняет большую работу, чем
при переходе пути ВbС. Следовательно, работа, которую выполняет система
при переходе из одного состояния в другое, зависит от пути перехода. Поскольку ΔU в уравнении (7.9) является величиной постоянной для данных начального
и конечного состояний, а количество выполняемой работы не является величиной постоянной и
зависит от пути, то очевидно, что количество теплоты, которую надо выдать
системе, чтобы переход состоялся, также зависит от пути перехода. Как следует из
(7.9), для перехода из состояния В в состояние С путем ВаС система должна получить большую
количество теплоты, чем для перехода путем ВbС.
Итак, как работа, выполненная системой,
так и количество теплоты, которую получает система при переходе из одного состояния в
другой, зависят от пути перехода.
Вполне понятно, что приведенные
рассуждения остаются в силе и тогда, когда система при переходе отдает теплоту
или когда над системой производится работа.
Таким образом, когда известны только
начальное и конечное состояния системы, а путь, по которому состоялся переход, неизвестный,
то нельзя ничего сказать о том, сколько энергии система получила (или
потеряла) в результате работы и сколько от нагрева: количество работы и
количество теплоты не являются функциями состояния термодинамической системы. Следовательно, содержание
первого принципа термодинамики можно раскрыть с помощью внутренней энергии
системы и двух единственно возможных эквивалентных форм передачи энергии - работы и
теплоты.