ОКИСЛЕНИЯ
И ВОССТАНОВЛЕНИЕ
2. Коррозия
2.1. Кислотная коррозия
Водные
растворы кислот нельзя перевозить или хранить в металлических емкостях, потому что они
могут вступать в реакцию с кислотой, и в результате этого могут протекать.
Пример.
Хлоридная кислота реагирует с железом с выделением водорода:
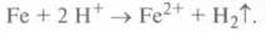
Реакция
металлов с ионами гідроксонію1 является окислительно-восстановительной реакцией: атом
металла отдает электроны, т.е. окисляется, а протон получает электрон, т.е.
восстанавливается. Такие металлы, как, например, медь, серебро и золото такой коррозии
не поддаются, поскольку они в меньшей степени способны отдавать электроны, чем
водород.
С
другой стороны, соединения этих металлов имеют склонность окислять водород и другие
металлы.
Водород
и металлы имеют разную способность отдавать электроны. Согласно их ионы имеют
разную способность получать электроны. На этой основе можно записать
окислительно-восстановительный ряд:

Металлы,
которые имеют меньшее разрешение, чем водород, отдавать электроны, называют
благородными металлами. Металлы, которые имеют большую способность, чем водород, отдавать
электроны, называют неблагородными металлами.
Запомните:
предметы из неблагородных металлов окисляются под воздействием кислых жидкостей. Этот
процесс называют кислотной коррозией.
__________________________________________________________________
1 Для упрощения
рассматривается как протон (Н+).