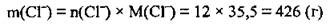РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
6. Смеси веществ. Растворы
Примеры решения типовых задач
Задача 1. Составьте молекулярное уравнение, соответствует таком сокращенном йонно-молекулярному уравнению:
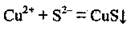
Решение
Йонно-молекулярное уравнение реакции показывает, что во время реакции состоялось связывания ионов Купруму Сu2+ и сульфид-ионов S2- в нерастворимое соединение купрум(II) сульфид CuS, то есть фактически реакция состоялась между ионами Сu2+ и S2-. Для того чтобы предложить молекулярное уравнение, надо определиться, между представителями которых классов неорганических веществ прошла реакция. Возможны такие варианты: 1) основание и кислота, 2) соль и кислота, 3) две соли.
От первого варианта откажемся сразу, поскольку купрум(ІІ) гидроксид есть нерозчинною основой и не диссоциирует с образованием иона Сu2+. Второй вариант так Же неприемлем, поскольку сероводород H2S плохо растворяется в воде и сероводородная кислота проявляет низкую степень диссоциации (К = 6,9 · 10-7 моль/л). Соответственно в растворе содержится незначительное количество сульфид-ионов, следовательно, такая реакция не произойдет. Остановимся на обменной реакции между двумя солями. Поскольку такие реакции происходят между двумя растворимыми в воде солями, то используем таблицу растворимости кислот, солей и оснований в воде (см. Приложения). Возможно использовать такие растворимые соли Сu2+: хлорид - СuСl2, бромид - CuBr2, сульфат - CuSO4 или нитрат - Сu(NO3)2. Среди сульфидов растворимыми в воде являются: калий сульфид - K2S, натрий сульфид - Na2S, аммоний сульфид - (NH4)2S, литий сульфид - Li2S. Запишем молекулярное уравнение:
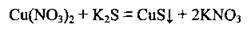
А теперь составим йонно-молекулярные уравнения:
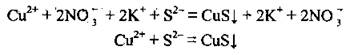
Полученный результат подтверждает правильность отбора солей и написание молекулярного уравнения.
Задача 2. Укажите пару формул веществ, которые нужно использовать, чтобы реакция состоялась согласно йонно-молекулярного уравнения:
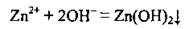
A Zn и Н2O
Бы ZnO и Н2O
В Zn3(PO4)2 и КОН
Г Zn(NO3)2 и NaOH
Решение
Приведенное йонно-молекулярное уравнение показывает, что,сущность реакции сводится к связыванию ионов Zn2+ и OН-. Ионы Zn2+ в растворе могут образоваться только благодаря диссоциации солей Цинка, которые растворимы в воде. Поскольку Zn3(PO4)2 в воде не растворяется, годится только вариант Г (Zn(NО3)2). А ионы ОН- образуются при диссоциации щелочей (NaOH):
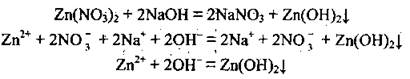
Задача 3. Укажите ионы, которые могут одновременно быть в растворе:
А Ва2+ и SO42-
Бы Ag+ и Сl-
В Na+ и SO42-
Г Ag+ и S2-
Решение
Ионы Na+ и SO42- могут содержаться в растворе одновременно, как угодно долго, потому что они не связываются в осадок, газ или малодисоційовану вещество, в отличие от других пар ионов:
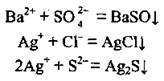
Правильным является ответ В.
Задача 4. Укажите ионы, которые не могут одновременно быть в растворе:
A NH4+ и SO42-
Б NH4+ и Сl-
B Mg2+ i PO43-
Г К+ и PO43-
Решение
Ионы, которые, взаимодействуя, образуют газ, осадок или малодисоційовану вещество, не могут одновременно содержаться в растворе. Ионы Mg2+ и РО43- связываются в нерастворимую в воде соль:
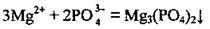
Правильным будет ответ.
Задача 5. Укажите массу хлорид-ионов в растворе алюминий хлорида с содержанием соли 4 моль/л. Считать, что соль подвергается полной диссоциации.
Решение
1. Напишем уравнение диссоциации соли:
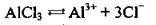
Из уравнения видно, что при диссоциации 1 моль соли образуется 3 моль хлорид-ионов. Соответственно при диссоциации 4 моль АlСl3 образуется 12 моль ионов хлора (Сl-). Для вычисления массы ионов воспользуемся формулой:
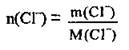
2. Из формулы вычисляем массу ионов. М(Сl-) = 35,5 г/моль: