Часть 2 МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
Раздел 7 ОСНОВЫ ТЕРМОДИНАМИКИ
7.1. Параметры термодинамической системы. Состояние системы. Процесс
Термодинамика изучает физические процессы
с точки зрения преобразования энергии, что происходит в них с учетом двух форм
ее передачи: работы и теплообмена. Однако, в отличие от
молекулярно-кинетической теории, термодинамика изучает макроскопические свойства
тел и явлений природы, оставляя без внимания их внутреннее строение. Не рассматривая
молекул и атомов, минуя микроскопический рассмотрение процессов, термодинамика дает
возможность сделать выводы относительно их протекания.
Термодинамика основывается на нескольких
фундаментальных законах, которые называют принципами термодинамики и которые являются
обобщением результатов многочисленных опытных фактов. Вследствие этого выводы термодинамики
имеют достаточно общий характер.
Термодинамика рассматривает широкий круг
явлений. Законы термодинамики можно применять к процессам, происходящим в
гальванических элементах, в магнитных явлений, процессов внутри звезд и др.
Вообще нет такой области физики и химии, в которой нельзя было бы применить
термодинамический метод. Бурное развитие термодинамики, становления ее как
науки приходится на XVIII - первую половину XIX вв. В механике Ньютона различные
процессы и закономерности объясняли с помощью «силы». Это понятие было
основным. В термодинамике аналогичную роль играет понятие «энергия».
Термодинамическая система состоит из
тел, взаимодействие которых со средой заключается в обмене энергией за работу и
за нагрева. Средой считаются все тела, окружающие систему, но к ее
состав не входят. Примером термодинамической системы может быть газ или вода и
пара над ней в закрытом сосуде.
Физическое состояние системы
характеризуется совокупностью числовых значений физических величин, которыми
определяются свойства системы. Такими величинами являются давление, температура, объем,
диэлектрическая проницаемость, показатель преломления света и т.д.
В термодинамике для характеристики
состояния системы обычно пользуются следующими тремя величинами: давлением р, объемом
V и температурой Т. Эти величины называются параметрами термодинамической
системы. При этом параметры могут быть внутренними, которые касаются этой
системы, и внешние, характеризующие внешние тела. Например, объем газа
считается внешним параметром, поскольку он зависит от размеров сосуда.
Давление газа - внутренний параметр, он зависит от средней кинетической энергии
молекул [формула (6.13)]. Для характеристики
термодинамического состояния смесей используют параметр, который называется
концентрацией. Параметры состояния связаны между собой так, что при изменении одного из
них изменяется по крайней мере еще один. Связь между параметрами состояния термодинамической
системы можно выразить, как отмечалось ранее, уравнением состояния. В простейшем
случае для идеального газа зависимость между объемом, давлением и температурой
выражается уравнением Менделеева - Клапейрона. Если параметры состояния
термодинамической системы имеют вполне определенное значение и с течением времени не изменяются при
неизменных внешних условиях, то такая система находится в состоянии равновесия. Когда же
параметры состояния меняются со временем, то в системе происходит термодинамический
процесс. Примером термодинамического процесса может быть изменение объема газа,
сопровождается изменением давления и температуры.
Равновесное состояние системы можно
изобразить графически точкой на плоскости с прямоугольными координатами, если
отложить по координатных осях значения любых двух параметров.
Неравновесное состояние нельзя так показать, поскольку в этом случае хоть один из параметров
не будет иметь определенного значения.
Графически можно изобразить только
равновесное состояние системы. Если термодинамическое состояние системы характеризуется
сначала точкой А, а затем точками В и С на диаграмме, то это означает, что система
перешла из одного состояния в другое (рис. 7.1). Следовательно, в системе происходит определенное
процесс.
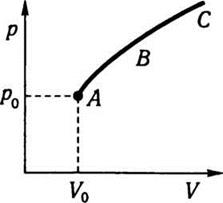
Рис. 7.1
Любой процесс, т.е. переход
системы из одного состояния в другое, связанный с нарушением равновесия в системе.
Следовательно, если в системе будет происходить процесс, то она будет проходить
через последовательность неравновесных состояний.
Процесс называют равновесным, если
система в любой момент времени находится в состоянии равновесия. Практически до
равновесного процесса приближаются такие процессы, которые
происходят очень медленно. Если в системе будет происходить такой процесс, то
система проходит через ряд бесконечно близких друг к другу состояний, а
точка, изображающая состояние, перемещается по какой-то кривой (например, по
кривой АВС).
Обратимым называют такой процесс,
который происходит в обоих направлениях (например, АВС-СВА) так, что система
возвращается в исходное положение без каких-либо изменений в окружающей среде.
Для необратимых процессов это требование нарушается. В основу классификации
термодинамических процессов можно положить признак неизменности любого из
параметров состояния. Термодинамический процесс называют ізобарним, если остается
постоянным давление, ізохорним - когда не меняется объем, изотермическим - при постоянной
температуры. Процесс, происходящий без теплообмена с внешней средой,
называют адиабатическим. Круговым процессом, или циклом, называют такой процесс,
при котором система выходит из какого термодинамического состояния и, претерпев изменений,
возвращается до того самого состояния.