Белки
Белки - это макромолекулярные органические соединения (биополимеры), структурную основу которых составляют полипептидные цепи, построенные из остатков α-
аминокислотыт.
В построении белковых молекул участвуют двадцать

-аминокислот. Белки имеют несколько уровней пространственной организации.
Первичная структура белка - это последовательность аминокислот в поліпептидному цепи.
Вторичная структура - образование поліпептидним цепью

-спирали или
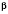
-слоя.
Третичная структура - пространственная укладка полипептидной цепи.
Четвертичная структура - объединение нескольких полипептидных цепей с третичным структурой.
Разнообразие белков, их значение в природе. Белки входят в состав всех живых организмов. Они выполняют множество функций, в том числе строительную и ферментативную.
Физические свойства белков. Одни белки растворимы, другие - нет. Много белков образуют коллоидные растворы. Белки имеют разный вкус, цвет и запах. Температуры, при которых происходит разрушение белка, специфические для каждого из них.
Химические свойства белков.
1) Под действием некоторых факторов происходит разрушение трехмерной структуры белка - денатурация, связанное с изменением четвертичной, третичной и вторичной структур; денатурация может быть обратимой и необратимой.
Факторы, которые вызывают денатурации белков:- нагрев;
- излучения, например инфракрасное или ультрафиолетовое;
- сильные кислоты, сильные щелочи, концентрированные растворы солей (в случае длительного действия разрываются даже пептидные связи);
- тяжелые металлы;
- органические растворители (использование спирта в качестве дезинфицирующего средства базируется на том, что он вызывает денатурации белков бактерий).
2) Важнейшее химическое свойство белков - способность к
гидролиз, который может проходить при нагревании с сильными кислотами или щелочами
(
кислотно-основной гідроліс),
а также под действием ферментов
(
ферментативный гідроліс). Гидролиз приводит к разрыву пептидных связей с образованием свободных аминокислот. Например, кислотный гидролиз:
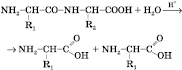
где R1 и R2 - радикалы аминокислот.
3)
Качественные цветные реакции билкив
:-
биуретовая реакция на пептидные связи - действие разбавленного раствора купрум(II) сульфата на слабощелочных раствор белка, сопровождается появлением фиолетово-синей окраски раствора;
-
ксантопротеїнова реакция на ароматические и гетероядерні циклы - действие концентрированной азотной кислоты с появлением желтой окраски.