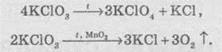|
Атомы
Хлора входят в состав кислот, находясь в разных степенях окисления. У всех
кислотах окисником могут выступать атомы Водорода или Хлора:
В
ряде НСlO-НСlO2-НСlO3-НСlO4 окислительные
свойства атома Хлора уменьшаются, а кислотные свойства, наоборот,
увеличиваются. Характеристика всех оксигеносодержащих кислот Хлора подана в
таблицы. Калий
хлорат Калий
хлорат КСlO3,
или бертолетовая соль (названа в честь французского химика Карла Бертолле,
впервые ее добыл), представляет собой бесцветное кристаллическое вещество, умеренно
растворимый в воде. Калий
хлорат добывают растворением хлора в горячем растворе калий гидроксида:
Расписание
бертолетовой соли при нагревании происходит в двух различных направлениях:
Бертолетовую
соль применяют при производстве спичек (в головках спичек содержится 47%
бертолетовой соли), в пиротехнических составах, как инсектицид в сельском
хозяйстве, а также для добывания кислорода в лабораториях. Хлорная известь Хлорная
известь, или білильне известь, или «хлорка» - это кальций хлорид-гипохлорит СаСl(ОСl), бесцветное кристаллическое соединение, в
сыром воздухе запах хлора. Это соединение получают при действии молекулярного
хлора в суспензию кальция гидроксида в воде:
При
действия кислот на раствор хлорной извести выделяется хлор:
Кальций
хлорид-гипохлорит применяют как отбеливающий средство для тканей и бумаги, для
дезинфекции, как средство для очистки воздуха и как окислитель в различных химических
синтезах. Фтороводорода При
взаимодействия фтора и водорода образуется фтороводорода HF. При нормальных условиях - бесцветная жидкость (Тпл
= -83 °С, Ткип = +20 °С) с резким запахом.
Высокие
температуры плавления и кипения объясняются тем, что молекулы HF сильно ассоциированы за счет образования
водородных связей, более прочных, чем связи между молекулами воды. В жидком
состоянии молекулы HF почти все димеризовані в молекулы H2F2. Фтороводорода
обычно получают действием серной кислоты на кальций флуорид (минерал флюорит):
Раствор
фтороводню в воде представляет собой кислоту средней силы (Ка =6,67 ∙ 10-4). Такой раствор
называют плавиковой (фторидною) кислотой. Диссоциация этой кислоты проходит по
таким механизмом:
Плавиковая
кислота известна как единственная кислота, которая растворяет стекло, вследствие взаимодействия с
преобладающим компонентом стекла - силиция диоксидом. Это происходит за счет
того, что кремний флуорид, который образуется в результате реакции, является леткою
веществом, которая изымается из реакционного среды и тем самым не мешает
дальнейшему протеканию реакции:
Плавиковую
кислоту хранят только в пластиковых или свинцовых сосудах. Стеклянные
сосуды для ее хранения непригодны. Фтороводорода
применяют для травления стекла, удаления примесей песка при выплавке металлов
и добыча флуоридів. Большие количества фтороводню используют для синтеза
различных органических соединений. Фтороводорода
встречается в природе только в вулканических газах.
|
|