ГАЛОГЕНЫ
ВЗАИМОДЕЙСТВИЕ ГАЛОГЕНОВ С МЕТАЛЛАМИ
Химические свойства галогенов, т.е.
способность вступать в реакции, образовывать те или другие соединения, определяются
их местом в периодической системе. Каждый галоген практически завершает период, в
котором он находится.
Рассмотрим сначала образование
соединения одного из галогенов, а именно - Хлора с Натрием.
Электронная формула атома Натрия 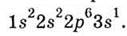 Он
имеет одну валентную АО
(Сs). Электронная
формула атома Хлора
Он
имеет одну валентную АО
(Сs). Электронная
формула атома Хлора 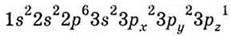 . У него тоже одна валентная АО (3рz). Эти валентные АО могут перекрываться с образованием молекулярной
орбитали, на которой размещаются два электрона. При этом из-за большой разницы в
размерах атомов Сl и Nа сочетаются, участок перекрывания АО смещена, и очень сильно, до атома
Хлора.
. У него тоже одна валентная АО (3рz). Эти валентные АО могут перекрываться с образованием молекулярной
орбитали, на которой размещаются два электрона. При этом из-за большой разницы в
размерах атомов Сl и Nа сочетаются, участок перекрывания АО смещена, и очень сильно, до атома
Хлора.
Через большую разницу в энергиях АО, перекрывающихся АО
(-496 кДж/моль для Сs-АО Натрия и -1250 кДж/моль для
Зр-АО Хлора), связующая МО, что образуется, мало отличается по энергии от АО атома Сl. Электрон атома Натрия,
расположен на более высокой Сs-АО, практически переходит на значительно
ниже Зр-АО атома Хлора.
Можно сказать, что атом Nа «отдал» свой электрон атому Сl, поэтому на атоме Na возникает положительный заряд, то есть он становится положительно
заряженным ионом. В свою очередь, атом Сl
«присоединяет» лишний электрон и превращается таким образом в отрицательно заряженный iон. Противоположно заряженные iоны Nа+ и Сl-
притягиваются друг к другу, образуя химическую связь между Натрием и Хлором:
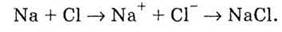
Или образующаяся при этом молекула NаСl? Здесь надо учесть, что електрозаряджена частица, в
том числе ион, может привлекать как угодно
многие другие, имеющие противоположный заряд, поэтому ивон натрия Nа+
притягивает к себе не один ион
хлора Сl-, а столько, сколько у него может
разместиться. Одновременно идентично ведет себя ион Сl-. В результате образуется
кристаллическая решетка из ионов Nа+ и Сl-.
Таким образом, вещество хлорид натрия,
его кристаллы, образованные не молекулами, а ионами. Такую же ионное строение имеют и
другие соединения металлов с неметаллами.
В отличие от веществ с
молекулярным строением (Н2, О2, F2,
Н2O и т. п.) ионные вещества имеют
значительно более высокие температуры плавления и кипения. Например, для поваренной соли NаСl tПЛ
= 801°С, tКИП = 1465 °С.