СТРОЕНИЕ АТОМА
ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМА
Химические свойства определяются
электронному строению атома.
Описать электронное строение атома - это
значит, прежде всего, отметить распределение электронной плотности около ядра, то есть
определить участок пространства, где могут находиться электроны данного атома.
Но для полного описания электронной
строения атома этого недостаточно. Важнейшей характеристикой движения электрона на
данной орбитали есть энергия притяжения его ядром или энергия связи его с
ядром.
В атоме Водорода энергия связи
электрона с протоном в расчете на 1 моль вещества составляет -1300 кДж.
(Энергии притяжения приписывается знак минус, потому что она пропорциональна произведению
величин зарядов притягиваются, знаки которых противоположны («+» и «-»), следовательно,
их произведение отрицательный).
Заряд ядра атома Гелия (+2) больший,
чем атома Водорода (+1). Значит, и энергия притяжения больше; поскольку два
электроны, имеющиеся в атоме Гелия, отталкиваются друг от друга, их энергия
связи с ядром меньше удвоенной энергии связи электрона в атоме Водорода и
составляет -2400 кДж/моль.
Усиление связи с ядром приводит
до приближения электронов к ядру, поэтому участок пространства, где движутся электроны
атома Не (то есть соответствующая орбиталь), более сжатая. Атом Гелия меньше атом
Водорода. Радиус сферы, где в основном находятся электроны, равна 0,06
нм.
Следующий по сложности строения -
атом Лития, что имеет три электроны. Два из них занимают такую же орбиталь, как и
электроны в атомах Н и Не (только эта орбиталь еще более сжата возле ядра). А
третьего электрона здесь быть не может. Напомним - на одной орбитали может быть не
более двух электронов, поэтому третий электрон должен находиться на другой орбитали.
Эта орбиталь также является сферой, только значительно большего радиуса.
Энергия связи с ядром третьего
электрона (в дальнейшем будем называть просто «энергия электрона») намного меньше
(по модулю), чем первых двух, что находятся к ядру ближе: значения энергий
составляют -520 и -7000 кДж/моль соответственно. В данном случае говорят, что
электрон находится на другом энергетическом уровне. Обозначим ближайший к
ядра уровень № 1, тогда третий электрон в атоме Лития находится на уровне № 2,
или просто - на 2-ом уровне.
Орбитали, имеющие сферическую форму,
называются s-орбіталями. В атоме Водорода
электрон находится на 1s-орбитали (1 - номер уровня, s - название орбитали). В атоме Не
оба электроны находятся на таком же 1s-орбитали. В атоме Lи два электрона занимают и один
электрон - 2s-орбиталь.
Теперь легко описать электронную
строение атома элемента, следующего за Литием, - Бериллия. У него есть четыре
электроны. Два из них занимают 1s-орбиталь и две - 2s-орбиталь. По сравнению с атомом Лития
атом Бериллия меньше, поскольку имеет большой заряд ядра, что сильнее сжимает
орбитали, чем в случае с Литием.
Таким образом, в атоме Бериллия 1sи 2s-орбитали оказываются полностью занятыми, поэтому в атоме
следующего элемента - Бора дополнительный пятый электрон должен занять новую
орбиталь.
В отличие от состояния электрона на
первом энергетическом уровне, на котором есть только одна орбиталь, а именно 1s, на втором уровне, более
удаленном от ядра, движение электронов может описываться двумя разными способами.
На втором энергетическом уровне есть два вида орбиталей. С одним из них вы уже
знакомые - это сферическая s-орбиталь. Другой вид орбиталей -
р-орбитали, имеющие форму объемной восьмерки (или гантели). На каждом
энергетическом уровне (кроме первого) есть по три р-орбитали, они взаимно
перпендикулярно ориентированные в пространстве вдоль осей х, у и z соответственно обозначаются рх, ру, рz.
На каждой р-орбитали (как и на s- и любых других) может находиться
не более двух электронов. Всего, таким образом, на 2-ом энергетическом уровне
может быть не более восьми электронов (два электрона на 2s-орбитали и по два электрона на
каждой из трех 2р-орбиталей), в отличие от первого уровня, где есть только одна
орбиталь.
р-Орбитали последовательно заполняются в
атомах следующих за Бериллием элементов: В,
... Вплоть до Неона Nе. Распределение электронов в атоме Неона (10 электронов) можно
записать формулой:
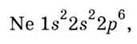
которая
означает, что на 1-ом уровне на 1s-орбитали находятся два электрона,
на 2-ом уровне на 2s-орбитали - два электрона и на
2р-орбиталях - шесть электронов.
Подан запись электронного строения
называется электронной формулой атома.
В атома следующего после Неона
элемента - Натрия - добавляется еще один электрон. Но все орбитали первых двух
уровней заполнены, и этот электрон занимает s-орбиталь 3-го уровня - Сs-орбиталь. Она находится еще дальше от ядра, энергия
связи этого электрона с ядром еще меньше, чем у электронов на 1sи 2s-орбиталях.