РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
4. Химическая реакция
4.8. Скорость химической реакции. Катализатор
Раздел химии, изучающий скорость химических реакций, называют химической кинетикой. Рассмотрим содержание некоторых понятий, которые используют в этом разделе.
Скорость химической реакции характеризуется изменением концентрации реагентов (или продуктов реакции) за единицу времени.
Если реакции происходят в однородной среде (например, реакции между газами или жидкостями), их называют гомогенными; если в неоднородном (например, между газом и твердым телом), то гетерогенными.
Во втором случае реакции происходят на поверхности соприкосновения веществ, которую называют поверхностью раздела фаз. Фаза - это часть системы, которая отделяется от других частей системы поверхностью раздела.
Скорость гомогенной реакции определяется количеством вещества, вступившего в реакцию или образовалась в результате реакции за единицу времени в единице объема:
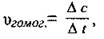
где vгомог. - скорость реакции в гомогенной системе, моль/с·м3 или моль/с·л;
Δс - изменение концентрации, моль/м3, моль/л;
Δt - интервал времени, с.
Скорость гетерогенной реакции определяется количеством вещества, вступившего в реакцию или образовалась в результате реакции за единицу времени на единице поверхности раздела фаз:
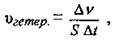
где vгетер. - скорость реакции в гетерогенной системе, моль/м2·с;
Δv = v1 - v2 - изменение количества вещества, моль;
S - площадь раздела фаз, м2;
Δt - интервал времени, с.
Скорость химической реакции зависит от различных факторов:
1) от природы реагентов. Например, металлы реагируют с хлоридной кислотой с разной скоростью: магний быстрее, чем железо, а медь не реагирует вообще:
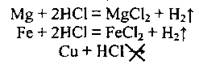
Галогены реагируют с водородом с разной скоростью: хлор скорее йод;
2) от концентрации реагентов (для веществ в жидкой и газообразной фазе). Например, реакция окисления нитроген(II) оксида чистым кислородом происходит быстрее, чем реакция окисления кислородом воздуха:
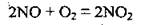
В 1865 г. М. М. Бекетов, а в 1867 г. К. Гульдберг и П. Вааге установили количественную зависимость скорости реакции от концентрации веществ, реагирующих. Эта зависимость выражается законом действующих масс: скорость химической реакции в каждый момент времени пропорциональна произведению концентраций реагентов.
Для простых одностадийных реакций концентрации веществ подносят к степени, который определяется стехиометрическим коэффициентом реагента. Например, для реакции
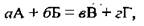
где а, б, в, г - коэффициенты,
A, b - формулы реагентов,
B, Г - формулы продуктов реакции,
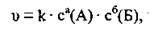
где v - скорость реакции,
сa(А), сб(Б) - молярные концентрации реагентов А и Б,
а, б - коэффициенты,
k - константа скорости.
Это выражение называют кінетичнім уравнением. Напомним, что в кинетические уравнения вводят только концентрации веществ, находящихся в газообразном и жидком состояниях. Например:
а) для реакции
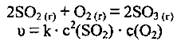
б) для реакции
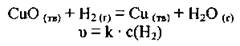
3) от площади поверхности реагентов (когда один из реагентов находится в твердой фазе). Реакции происходят быстрее, если площадь поверхности веществ, которые реагируют, большая. Площади контакта веществ увеличивают, измельчая твердый реагент. Например, сахар (сахар-песок или кусочек рафинада) горит только в пламени, а сахарная пудра вспыхивает от искры1;
4) от температуры - правило Вант-Гоффа2: с повышением температуры на каждые 10 °С скорость большинства химических реакций увеличивается в 2-4 раза:
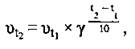
где vt2 - скорость реакции при температуре t2,
vt1 - скорость реакции при температуре t1,
γ - температурный коэффициент (γ = 2...4).
Даже небольшое повышение температуры вызывает резкое увеличение скорости реакции. Это объясняется тем, что взаимодействовать могут лишь те частицы, энергия которых будет достаточным для ослабления или разрыва химических связей в исходных веществах. Такие частицы называют активными. При повышении температуры число активных частиц возрастает, соответственно возрастает и скорость реакции. Например, железо с хлором при комнатной температуре реагирует медленно, а при высоких температурах идет бурная реакция; водород вступает в реакцию с оксидами металлических элементов только во время нагрева:
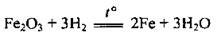
5) от наличия катализатора - вещества, которое изменяет скорость химической реакции (но само при этом не расходуется).
Так, синтез аммиака из азота и водорода происходит только при наличии железа со специальными добавками:
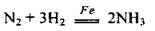
Реакция окисления аммиака кислородом происходит только при наличии платины:
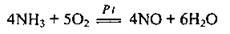
Химические реакции, которые происходят при участии катализаторов, называют каталитическими, а само явление изменения скорости реакции при наличии катализатора - катализом3.
Одни вещества увеличивают скорость реакции (положительный катализ), их называют катализаторами. Другие вещества уменьшают скорость реакции (отрицательный катализ), их называют ингибиторами. Большинство химических реакций, которые происходят в природе, является каталитическими. Наиболее известным и распространенным катализатором является вода. Живые системы используют биологические катализаторы, которые имеют белковую природу; их называют ферментами (энзимами).
Различают гомогенный и гетерогенный катализ.
Гомогенный катализ происходит при наличии катализатора, который находится в таком же агрегатном состоянии (в одной фазе), что и реагенты (жидком или газообразном). О гетерогенный (контактный) катализ говорят тогда, когда реагенты и катализатор находятся в разных агрегатных состояниях, то есть в разных фазах (катализатор обычно твердый, а реагенты - жидкие или газообразные).
|
Гомогенный катализ
|
Гетерогенный катализ
|
|
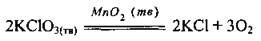
|
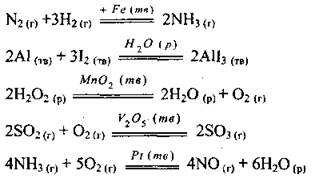
|
Считают, что катализатор образует с реагентами промежуточные соединения. Например, реакция
А + В = АВ
без катализатора происходит очень медленно. Если использовать катализатор К, то он вступит в реакцию с одним из реагентов, образовав промежуточное соединение АК:
А + К = АК,
значительно активнее за вещество А и легко взаимодействует с веществом В:
АК + В = АВ + К
Таким образом катализатор не входит в состав конечных продуктов реакции, а следовательно, его количество остается неизменной.
_____________________________________________________________________
1 Способны к окислению вещества, измельченные в порошок, являются взрывоопасными: мука, угольная пыль и т.п. могут самопроизвольно (при отсутствии искры или открытого пламени) вспыхивать и взрываться.
2 Эмпирическое правило, которое на основе многих экспериментов вывел голландский химик Якоб Хендрик Вант-Гофф (1852-1911), первый лауреат Нобелевской премии по химии, 1901 г. Правило действует лишь в нешироком температурном диапазоне (от 0 до 100 °С).
3 Термин «катализ» ввел 1835 г. шведский химик Йонс Якоб Берцелиус (1779-1848).