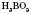|
2) по наличию Кислорода в кислотном остатке - на безоксигенові и кислородосодержащие. Оксигенові кислоты
Безоксигенові кислоты
Получение кислот1) Кислородосодержащие растворимые в воде кислоты можно получить взаимодействием оксидов с водой: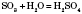 2) Оксигеновмисні нерастворимые в воде кислоты получают взаимодействием соответствующей соли более сильной кислотой: 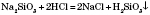 3) Бескислородные кислоты получают взаимодействием водорода с неметалом: 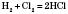 с последующим растворением продукта реакции в воде. Физические свойства кислотБольшинство кислот - жидкости, но есть и твердые кислоты, например ортофосфатная и метафосфатна, силикатный. Все кислоты тяжелее воды и в большинстве случаев хорошо в ней растворяются. Некоторые летучие кислоты (хлоридная, нитратная) имеют характерный запах. Почти все кислоты бесцветные.Химические свойства кислот1) Действие на индикаторы. Вещества, которые изменяют свою окраску под действием кислот или щелочей, называются индикаторами.2) Взаимодействие с металлами. Металлы, стоящие в ряду напряжений до Водорода, вытесняют его из разбавленных кислот (кроме азотной кислоты): 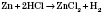 3) Кислоты реагируют с оксидами, образованные металлами: 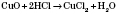 Реакции обмена - это реакции между двумя сложными веществами, в результате которых они обмениваются своими составными частями. 4) Кислоты реагируют с основаниями: 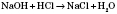
|
|
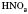
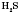 ,
, 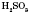
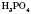 ,
,