ЭНЕРГЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ
3. Движущая сила химических реакций
3.5.
Возвратность реакции
В соответствии
уравнение Гиббса-Гельмгольца, свободная энергия реакции ∆G0R зависит от температуры. Если не
учитывать зависимость от температуры ∆H0R и
∆S0R, то
уравнение Гиббса-Гельмгольца соответствует уравнению прямой.
В зависимости
от знаков ∆H0R и
∆S0R различают
четыре типа реакции.
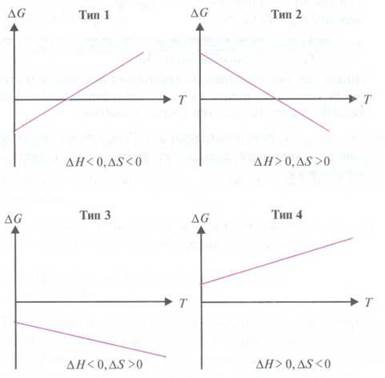
Тип
1: при температуре Т Т0 происходит спонтанная реакция -
екзоергічна реакция. При Т > Т0 реакция спонтанно не проходит,
это - ендоергічна реакция.
Тип
2: при температуре Т Т0 реакция спонтанно не происходит, это -
ендоергічна реакция. При Т > Т0 проходит спонтанная реакция -
екзоергічна реакция.
Тип
3: при любых температурах реакция екзоергічною.
Тип
4: при любых температурах реакция ендоергічною. Температуру Т0
называют температурой инверсии. При этой температуре спонтанное прохождение
реакции прекращается.
Пример.
Реакция гидроген хлорида и аммиака с образованием аммоний хлорида происходит
по типу 1.
При
температуре инверсии Т0 - ∆GR = 0.
Отсюда:
∆HR - T0∆Sr =
0,
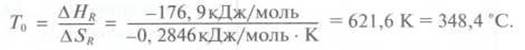
Ниже
от этой температуры спонтанно происходит образование аммоний хлорида, выше -
спонтанное разложение аммоний хлорида на водород хлорид и аммиак.
Запомните:
при температуре Т = Т0 вещества, участвующие в возможной
реакции, не реагируют - реакция не происходит.