Часть И. ОБЩАЯ
ХИМИЯ
Раздел 2. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И СТРОЕНИЕ АТОМОВ
§
2.10. Периодические свойства атомов
Такие свойства атомов, как размер,
энергия ионизации, сродство к электрону, электроотрицательности, степень
окисления, связанные с электронной конфигурацией атома. В их изменении со
увеличением порядкового номера элемента прослеживается периодичность.
Атомы не имеют четко определенных границ,
что обусловлено волновой природой электронов. В расчетах пользуются так
называемыми эффективными, или мнимыми, радиусами, то есть радиусами шаровидных
атомов, сблизились между собой во время образования кристалла. Конечно их
вычисляют по рентгенометричними данным.
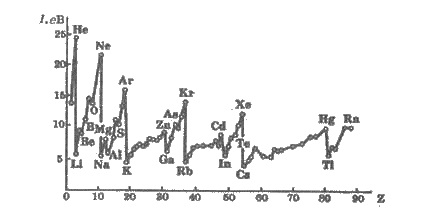
Рис. 2.6. Изменение энергии ионизации
атома в зависимости от порядкового номера элемента
Радиус атома - важная его характеристика.
Чем больше атомный радиус, тем слабее удерживаются внешние электроны. И
наоборот, с уменьшением атомного радиуса электроны притягиваются к ядру
сильнее.
В периоде атомный радиус вообще
уменьшается слева направо. Это объясняется увеличением сил притяжения электронов
с ростом заряда ядра. В подгруппах сверху вниз атомный радиус возрастает,
поскольку вследствие добавления дополнительного электронного слоя увеличивается объем
атома, а значит, и его радиус.
Энергия ионизации - это энергия,
необходима для отрывания самое слабое связанного электрона от атома. Она
обычно выражается в электрон-вольтах. Вследствие отрывание электрона от
атома образуется соответствующий катион.
Энергия ионизации для элементов
одного периода возрастает слева направо с увеличением заряда ядра. В подгруппе
она уменьшается сверху вниз вследствие увеличения расстояния электрона от ядра.
Изменение энергии ионизации атомов с увеличением заряда ядра графически изображена на
рис. 2.6.
Энергия ионизации связана с
химическими свойствами элементов. Так, щелочные металлы, энергия ионизации которых
малая, имеют ярко выраженные металлические свойства. Химическая инертность
благородных газов связана с их большими значениями энергии ионизации.
Атомы могут не только отдавать, но и присоединять электроны. При этом
образуется соответствующий анион. Энергия, которая выделяется в результате присоединения к
атома одного электрона, называется сродством к электрону. Конечно,
сродство к элек трона, как и энергию ионизации, выражают в
электрон-вольтах. Величина сродства к электрону известна не для всех
элементов; измерять ее довольно трудно. Наибольшие значения этих величин имеют
галогены, в которых на внешнем уровне расположены по 7 электронов. Это свидетельствует
о усиление неметаллических свойств элементов по мере приближения к концу
периода.
Определение электроотрицательности дал
американский ученый Л. Полинг в 1932 г. Он также предложил и первую шкалу
электроотрицательности. За Полингом, электроотрицательности - это способность атома в
соединении притягивать к себе электроны.
Имеются в виду валентные электроны,
то есть электроны, участвующие в образовании химической связи. Очевидно, в
благородных газов электроотрицательности нет, поскольку внешний уровень в их
атомах завершен и стойкий.
Для количественной характеристики
предложено принять за меру электроотрицательности энергию, которая равна
арифметической сумме энергии ионизации атома (l) и сродства электрона (E), т.е.
X = l
+
Е,
(2.3)
где
X -
электроотрицательности атома, а следовательно, и элемента.
В качестве примера определим X для фтора и
лития. Из справочных таблиц находим, что lF = 17,42 эв, EF
= 3,62 эв, lLи = = 5,39 эв, ELи = 0,22 эв (вычислены косвенным
способом). Тогда ХF
= 17,42 + 3,62 = 21,04 эв, а ZLи
= 5,39 + 0,22 = = 5,61 эв.
Фтора имеет наибольшее значение l + E, поэтому он является наиболее
електронегативним элементом. Наименьшие значения электроотрицательности атомы имеют
щелочных металлов.
Конечно электроотрицательности лития
принимают за единицу и сравнивают с ней электроотрицательности других элементов.
Тогда достают простые и удобные для сравнения величины относительной
электроотрицательности элементов (обозначим ее через х):
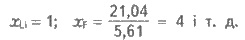
Сейчас широко используют таблицу
относительных электроотрицательностей, в которую вошли последние данные об электронной
строение атомов и их радиусы (табл. 2.2).
Таблица 2.2.
Относительные электроотрицательности элементов
|
|
И
|
II
|
III
|
IV
|
V
|
VI
|
VII
|
VIII
|
|
И
|
H
2,1
|
|
|
|
|
|
|
|
He
-
|
|
II
|
Li
0,97
|
Be
1,47
|
В
2,01
|
C
2,50
|
N
3,07
|
O
3,5
|
F
4,10
|
|
Ne
-
|
|
III
|
Na
1,01
|
Mg
1,23
|
Al
1,74
|
Si
1,47
|
P
2,1
|
S
2,6
|
Cl
2,83
|
|
Ar
-
|
|
|
К
0,91
|
Ca
1,04
|
Sc
1,20
|
Те
1,32
|
V
1,45
|
Cr
1,56
|
Mn
1,60
|
Fe
1,64
|
Co
1,70
|
Ni
1,75
|
|
|
IV
|
Cu
1,75
|
Zn
1,66
|
Ga
1,82
|
Ge
2,02
|
As
2,20
|
Se
2,48
|
Br
2,74
|
|
Kr
-
|
|
|
Rb
0,89
|
Sr
0,99
|
Y
1,11
|
Zr
1,22
|
Nb
1,23
|
Mo
1,30
|
Tc
1,36
|
Ru
1,42
|
Rh
1,45
|
Pd
1,35
|
|
|
V
|
Ag
1,42
|
Cd
1,46
|
In
1,49
|
Sn
1,72
|
Sb
1,82
|
То
2,01
|
l
2,21
|
|
Xe
-
|
|
|
Cs
0,86
|
Ba
0,97
|
La*
1,08
|
Hf
1,23
|
И
1,33
|
W
1,40
|
Re
1,46
|
Os
1,52
|
lr
1,55
|
Pt
1,44
|
|
|
VI
|
Au
1,42
|
Hg
1,44
|
Те
1,44
|
Pb
1,55
|
Bi
1,67
|
Po
1,76
|
At
1,90
|
|
Rn
-
|
|
VII
|
Fr
0,86
|
Ra
0,97
|
Ac**
1,00
|
* Лантаноїди 1,08-1,14
**Актиноїди
1,11-1,2
|
Следует отметить, что значение
относительных электроотрицательностей, которые приводятся в различных книгах по химии, несколько
отличаются. Это объясняется тем, что их рассчитывали различными методами,
исходя из определенных предположений и догадок.
Сопоставляя значение электроотрицательностей
элементов от францию (0,86) до фтора (4,10) (см. табл. 2.2), легко заметить,
относительная электроотрицательности подлежит периодическому закону: в периоде она
возрастает с увеличением номера элемента, в группе -
уменьшается. Ее значение является мерой неметапічності элементов. Очевидно, чем больше
относительная электроотрицательности, тем сильнее элемент проявляет неметаллические
свойства.
Из табл. 2.2 также видно, что неметаллы
характеризуются большой относительной електронегативністю, а металлы - небольшой.
Во время химического взаимодействия элементов электроны смещаются от атома с меньшей к
атому с большей относительной електронегативністю.
О степень окисления см. § 3.9.