Понятие об растворы и растворимость
Растворы - однородные системы, состоящие из двух и более компонентов и продуктов их взаимодействия. Растворы относятся к
однородных растворои. Так, водные растворы состоят из
растворителя (воды),
растворенного вещества и продуктов их взаимодействия -
гидратированных (соединенных с молекулами воды)
йонив.
Растворимость - способность вещества растворяться в воде или другом растворителе.
Количественно растворимость выражают как отношение массы растворенного вещества в насыщенном растворе до 100 г (или 1 л) воды (при данной температуре). Эта величина называется
коэффициентом розчинности
, или
розчинністю.
Вода - полярный растворитель
В молекуле воды связи между атомами Кислорода и Водорода ковалентные полярные, электронная плотность смещена в сторону Кислорода, как более электроотрицательного элемента. На атоме Кислорода вследствие этого накапливается отрицательный заряд, а на атомах Водорода - положительный.
Поэтому молекула воды полярная, она называется
диполем (два полюса - положительный и отрицательный).
По растворимостью в воде все вещества можно разделить на три группы:
1)
хорошо растворимые - в 100 г воды при комнатной температуре растворяется более 10 г вещества;
2)
малорастворимые - в 100 г воды при комнатной температуре растворяется менее 1 г вещества;
3)
практически нерастворимые - в 100 г воды при комнатной температуре растворяется менее 0,1 г вещества.
Абсолютно нерастворимых веществ не существует.
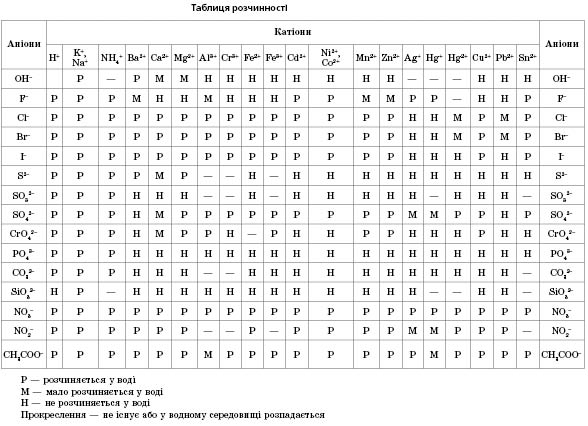
Растворимость кислот, солей и оснований в воде можно определить с помощью
таблицы розчинности
(см. с. 350)
Растворимость веществ зависит:
1) от природы розчинюваної вещества и растворителя;
2) температуры (от увеличения температуры растворимость твердых веществ и жидкостей увеличивается, газов - уменьшается);
3) давления (только для газов).
Растворы классифицируют как
насыщенные и
ненасичени,
концентрированные и
розбавлени.
Раствор, в котором при данной температуре вещество больше не растворяется, называется
насиченим.
Раствор, в котором розчинювана вещество еще может растворяться, называется
ненасиченим.