Часть И. ОБЩАЯ
ХИМИЯ
Раздел 2. ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА И СТРОЕНИЕ АТОМОВ
§
2.6. Строение электронных оболочек атомов
Теперь рассмотрим строение отдельно
взятого электронного уровня (слоя). Начиная со значения главного квантового
числа n
= 2, энергетические уровни (слои) делятся на подуровни (подслои),
отличаются друг от друга энергией связи с ядром.
Число подуровней равно главном
квантовому числу, но не может быть больше четырех: 1-й уровень имеет один
подуровень, 2-й - два, 3 - три, 4-й - четыре подуровня. Подуровни, в свою очередь,
состоят из орбиталей. Подуровни принято обозначать латинскими буквами: s
- первый, ближайший к
ядра подуровень каждого энергетического уровня, состоит из одной s-орбитали; г - второй подуровень,
состоит из трех р - орбиталей; d-третий подуровень, состоит из пяти d- орбиталей; f
- четвертый подуровень,
содержит семь f-орбиталей.
Таким образом, для каждого значения n существует n2 орбиталей (табл. 2.1).
Таблица
2.1. Главное квантовое число, типы и число орбиталей и максимальное число
электронов по подуровням и уровнях
|
Энергетический
уровень п
|
Число
подуровней, что равняется n
|
Орбиталь
|
Число
орбиталей
|
Максимальное
число электронов
|
|
на
подуровни
|
на
уровне,
что
равна
n
|
на
подуровни
|
на
уровне
|
|
К
(n
= 1)
|
1
|
1s
|
1
|
1
|
2
|
2
|
|
L (n = 2)
|
2
|
2s
|
1
|
4
|
2
|
8
|
|
|
|
2p
|
3
|
|
6
|
|
|
М(n = 3)
|
3
|
3s
|
1
|
|
2
|
|
|
|
|
Зр
|
3
|
9
|
6
|
18
|
|
|
|
3d
|
5
|
|
10
|
|
|
N (n = 4)
|
4
|
4s
|
1
|
|
2
|
|
|
|
|
4р
|
3
|
|
6
|
|
|
|
|
4d
|
5
|
16
|
10
|
32
|
|
|
|
4f
|
7
|
|
14
|
|
На каждой орбитали может находиться
не более двух электронов - принцип Паули. Если на орбитали находится один
электрон, то он называется неспаренным, если два, то это спаренные электроны. Принцип
Паули объясняет формулу N =
2n . И действительно,
если, например, на третьем уровне (n = 3) содержится 32=9 орбиталей, а на каждой орбитали -
по 2 электрона, то максимальное число электронов составляет 2 ∙ 32 = 18.
В табл. 2.1 для первых четырех
уровней показана связь главного квантового числа n с числом подуровней, типом и числом
орбиталей и с максимальным числом электронов на подуровне и уровне, а на рис.
2.3 приведена схема разделения энергетических уровней на подуровни. Из таблицы следует,
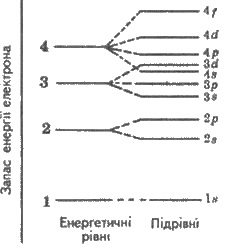
Рис. 2.3. Схема разделения энергетических
уровней на подуровни
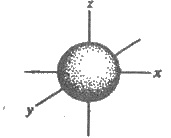
Рис. 2.4. Форма s-электронной орбитали
что
для характеристики электронов в атоме нужно знать номер электронного уровня и
типы орбиталей. Важно знать форму различных
орбиталей (облаков). Это необходимо при изучении структуры молекул. Согласно
теоретическими данными s-орбиталь
имеет сферическую симметрию, то есть форму шара. Примером может быть орбиталь атома
водорода, n
= 1 (рис. 2.4). Такую орбиталь называют s-орбіталлю. Электрон, который находится
на s-орбитали,
называется s-электроном.
На втором энергетическом уровне (n = 2) есть 4 орбитали, причем одна из
них имеет сферическую симметрию. Она называется 2s-орбіталлю. Очевидно, 2s-электрон имеет высшую энергию, а потому
будет находиться дальше от ядра, чем 1s-электрон. Вообще, для
каждого значения n существует одна орбиталь симметрична.
р-Орбиталь имеет форму гантели, или
объемной восьмерки (рис. 2.5). Все три р-орбитали расположены в атоме взаимно
перпендикулярно. Они направлены вдоль осей пространственных координат, поэтому их
часто обозначают как рх-, pв- и гz- орбитали. Такое обозначение указывает
на пространственную направленност р-орбиталей. Если рх-орбиталь расположена в направлении
оси х, то, очевидно, pх-электрон
с наибольшей вероятностью будет находиться вблизи оси х. То же самое можно сказать и
о орбитали рв и pz.
Следует отметить, что каждый
энергетический уровень (слой), начиная с n=2, имеет три р-орбитали. С
увеличением n-электроны
занимают р-орбитали, расположенные на больших расстояниях от ядра, но
направленност их по осям х, у, z всегда
хранится. Еще более сложные формы, чем р-орбитали, имеют d-орбитали (их пять) и f-орбитали (их семь). Здесь они не
рассматриваются.
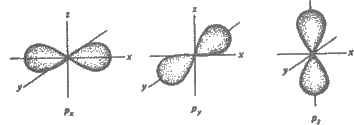
Рис. 2.5. Форма и ориентация
р-электронных орбиталей