ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ, ВХОДЯЩИЕ В СОСТАВ КЛЕТКИ.
Органические соединения составляют около 20-30 % массы живых клеток. К ним
относятся биологические полимеры - белки, нуклеиновые кислоты и полисахариды, а
также жиры, гормоны, пигменты, АТФ и т.д.
Белки составляют 10-18% от общей массы клетки (50 - 80% от сухой
массы). Молекулярная масса белков колеблется от десятков тысяч до многих
миллионов единиц. Белки - это биополимеры, мономерами которых являются аминокислоты. Все
белки живых организмов построены из 20
аминокислот. Не смотря на это, разнообразие белковых молекул огромно.
Они различаются по величине, структуре и функциям, которые определяются
количеством и порядком расположения аминокислот. Кроме простых белков (альбумины,
глобулины, гістони) есть и сложные, которые представляют собой соединения белков с углеводами
(глікопротеїди), жиры (липопротеиды) и нуклеиновыми кислотами
(нуклеопротеїди).
Каждая аминокислота состоит из углеводородного радикала, соединенного с
карбоксильною группой, имеет кислотные свойства (-СООН), и
аминогруппой (-NH2), которая имеет основные свойства. Аминокислоты
отличаются друг от друга только радикалами. Аминокислоты являются амфотерными
соединениями, которые имеют одновременно свойства и кислот, и оснований. Это явление
обусловливает возможность соединения кислот в длинные цепочки. При этом
устанавливаются прочные ковалентные (пептидные) связи между углеродом кислотной и азотом
основной групп (-CO-NH-) с выделением молекулы
воды. Соединения, состоящие из двух аминокислотных остатков, называются
дипептидами, с трех - трипептидами, из многих - полипептидами.
Белки живых организмов состоят из сотен и тысяч аминокислот, т.е.
есть макромолекулами. Различные свойства и функции белковых молекул определяются
последовательностью соединения аминокислот, которая закодирована в ДНК. Эту последовательность
называют первичной структурой молекулы белка, от которой, в свою очередь, зависят
дальнейшие уровни пространственной организации и биологические свойства белков.
Первичная структура белковой молекулы обусловлена пептидными связями.
Вторичная структура белковой молекулы достигается ее спіралізацією,
благодаря установлению между атомами соседних витков спирали водородных связей.
Они слабее ковалентных, но, много раз повторенные, создают достаточно прочную
соединение. Функционирования в виде закрученной спирали характерно для некоторых
фибриллярных белков (коллаген, фибриноген, миозин, актин и др).
Большинство белковых молекул становятся функционально активными только после
приобретение глобулярної (третичной) структуры. Она формируется путем
многократного сворачивания спирали в трехмерное образование - глобулу. Эта
структура сшивается, как правило, еще более слабыми дисульфидными (-S-S-)
связями. Глобулярну структуру имеет большинство белков (альбумины, глобулины
т.п.).
Для выполнения некоторых функций требуется участие белков с более высоким
уровнем организации, при котором возникает объединение нескольких белковых глобулярних
молекул в единую систему - четвертичну
структуру (химические связи могут быть разные). Например, молекула гемоглобина
состоит из четырех разных глобул и гемінової группы, содержащий ион железа.
Утрата белковой молекулой своей структурной организации называется
денатурацией. Причиной ее могут быть различные химические (кислоты, щелочи, спирт, соли
тяжелых металлов и др.) и физические (высокие температура и давление, ионизирующее
излучения и т.п.) факторы. Сначала разрушается очень слабая - четвертична,
затем третичная, вторичная, а при более жестких условиях и первичная структура. Если
под действием денатурирующего фактора не затрагивается первичная структура, то при
возврате белковых молекул в нормальные условия среды их структура полностью
восстанавливается, т.е. происходит ренатурации. Это свойство белковых молекул
широко используется в медицине для приготовления вакцин и сывороток и в
пищевой промышленности для получения пищевых концентратов. При необратимой
денатурации (разрушении первичной структуры) белки теряют свои свойства.
Белки выполняют следующие функции: строительную, каталитическую, транспортную,
двигательную, защитную, сигнальную, регуляторную и энергетическую.
Как строительный материал белки входят в состав всех клеточных мембран,
гіалоплазми, органоидов, ядерного сока, хромосом и ядрышек.
Каталитическую (ферментативную) функцию выполняют белки - ферменты, в
десятки и сотни тысяч раз ускоряя протекание биохимических реакций в клетках
при нормальном давлении и температуре около 37 °С. Каждый фермент может
катализировать только одну реакцию, то есть действие ферментов строго специфично.
Специфичность ферментов обусловлена наличием одного или нескольких активных
центров, в которых происходит тесный контакт между молекулами фермента и
специфического вещества (субстрата). Некоторые ферменты применяются в медицинской
практике и пищевой промышленности.
Транспортная функция белков заключается в переносе веществ, например
кислорода (гемоглобин) и некоторых биологически активных веществ (гормонов).
Двигательная функция белков заключается в том, что все виды двигательных реакций клеток
и организмов обеспечиваются специальными скоротливими белками - актином и
міозином. Они содержатся во всех мышцах, ресницах и джгутиках. их нити способны
сокращаться с использованием энергии АТФ.
Защитная функция белков связана с выработкой особых лейкоцитами
белковых веществ - антител в ответ на проникновение в организм чужеродных
белков или микроорганизмов. Антитела связывают,
нейтрализуют и разрушают не свойственные организму соединения. Примером защитной
функции белков может быть превращение фибриногена в фибрин при свертывании
крови.
Сигнальная (рецепторная) функция осуществляется белками благодаря способности
их молекул изменять свою структуру под воздействием химических и физических факторов,
вследствие чего клетка или организм воспринимает эти изменения.
Регуляторная функция осуществляется гормонами, которые имеют белковую природу
(например, инсулин).
Энергетическая функция белков заключается в их способности быть источником энергии
в клетке (как правило, при отсутствии других). При полном ферментативном
расщеплении 1 г белка выделяется 17,6 кДж энергии.
Углеводы. Углеводы, или сахариды, - органические вещества с общей
формуле Сn(Н20)m. В большинстве углеводов
число атомов водорода в два раза превышает количество атомов кислорода. Поэтому эти вещества
и были названы углеводами. В животных клетках углеводов немного - 1-2,
иногда до 5% (в клетках печени). Богаты углеводами растительные клетки, где их
содержание достигает 90% сухой массы (клубни картофеля).
Углеводы подразделяют на простые и сложные. Простые углеводы
называются моносахаридами. В зависимости от числа атомов углерода в молекуле
моносахариды называются триозами (3 атома), тетрозами (4 атома), пентозами (5
атомов) или гексозами (6 атомов углерода).
Из шести углеродных моносахаридов - гексоз - наиболее важны глюкоза,
фруктоза и галактоза. Глюкоза содержится в крови (0,1-0,12 %) и служит основным
источником энергии для клеток и тканей организма. Пентози - рибоза и
дезоксирибоза входят в состав нуклеиновых кислот и АТФ. Если в одной
молекуле объединяются два моносахариды, то такое соединение называют дисахаридом.
К дисахариду относится пищевой сахар, который получают из сахарного тростника
или сахарной свеклы. Он состоит из одной молекулы глюкозы и одной
молекулы фруктозы. Молочный сахар также является Дымером и включает глюкозу и
галактозу.
Сложные углеводы, образованные многими моносахаридами много кого,
называются полисахаридами. Мономером таких полисахаридов, как крахмал,
гликоген, целлюлоза, является глюкоза.
Углеводы выполняют две основные функции: строительную и энергетическую.
Например, целлюлоза образует стенки растительных клеток; сложный полисахарид
хитин - главный структурный компонент наружного скелета членистоногих.
Строительную функцию хитин выполняет и у грибов. Углеводы играют роль
основного источника энергии в клетке. В процессе окисления 1 г углеводов
освобождаются 17,6 кДж энергии. Крахмал у растений и гликоген у животных,
откладываясь в клетках, служит энергетическим резервом.
Липиды (жиры) и ліпоїди являются обязательными компонентами всех клеток. Жиры являются
сложными эфирами высокомолекулярных жирных кислот и спирта трьохатомного
глицерина, а ліпоїди - жирных кислот с другими спиртами. Эти соединения нерастворимы в
воде (гидрофобные). Липиды могут образовывать сложные комплексы с белками
(липопротеиды), углеводами (гліколіпіди), остатками фосфорной кислоты
(фосфолипиды) и т.п. Содержание жиров в клетке колеблется от 5 до 15% массы сухой
вещества, а в клетках подкожной жировой клетчатки - до 90%.
Жиры выполняют строительные/, энергетическую, запасаючу и защитную функции.
Бімолекулярний слой липидов (преимущественно фосфолипиды) образует основу всех
биологических мембран клеток. Липиды входят в состав оболочек нервных
волокон. Жиры являются источником энергии: при полном расщеплении 1 г жира
освобождается 38,9 кДж энергии. Они служат источником воды, выделяющейся при
их окислении. Жиры являются запасным источником энергии, накапливаясь в жировой
ткани животных и в плодах и семенах растений. Они защищают органы от
механических повреждений (например, почки окутаны мягким жировым «футляром»).
Накапливаясь в подкожной жировой клетчатке некоторых животных (киты, тюлени),
жиры выполняют функцию теплоизоляции.
Нуклеиновые кислоты имеют первостепенное биологическое значение и являются сложными
высокомолекулярными біополімерами, мономерами которых являются нуклеотиды. Они впервые
были найдены в ядрах клеток, откуда и их название (nucleus - ядро).
Существуют два типа нуклеиновых кислот: дезоксирибонуклеиновая (ДНК) и
рибонуклеиновая (РНК). ДНК входит в основном в хроматин ядра, хотя небольшое ее
количество содержится и в некоторых органоїдах (митохондрии, пластиди). РНК
содержится в ядрышках, рибосомах в цитоплазме клетки.
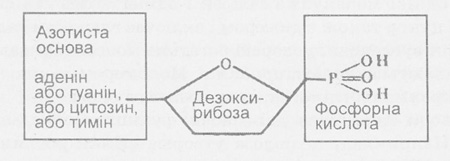
Рис. 127. Схема строения нуклеотида.
Структура молекулы ДНК была впервые расшифрована Дж. Уотсоном и Ф. Криком в
1953 г. Она является двумя полінуклеотидними цепями, соединенными друг с другом.
Мономерами ДНК являются нуклеотиды, в состав которых входят: п'ятивуглецевий сахар - дезоксирибоза,
остаток фосфорной кислоты и азотная основа.
Нуклеотиды отличаются друг от друга только азотными основаниями. К
состав нуклеотидов ДНК входят следующие азотистые основания: аденин, гуанин, цитозин
и тимин. Нуклеотиды соединяются в цепочку путем образования ковалентных связей
между дезоксирибозою одного и остатком фосфорной кислоты соседнего нуклеотида.
Оба цепочки объединяются в одну молекулу водородными связями, возникающими
между азотными основами различных цепочек, причем за определенную пространственную
конфигурацию между аденіном и тимином устанавливаются две связи, а между гуанином
и цитозином - три. Вследствие этого нуклеотиды двух цепочек образуют пары:
А-Т, Г-Ц. Четкое соответствие нуклеотидов друг другу в парных цепочках ДНК
называется комплементарністю (додатковістю). Это свойство лежит в основе
репликации (самоподвоєння) молекулы ДНК, то есть образования новой молекулы на
основе первоначальной.
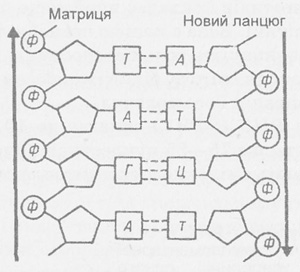
Рис. 128. Комплементарная соединение
нуклеотидов и образования дволанцюгової молекулы ДНК.
Репликация (от лат. replicatio - повторение) происходит следующим образом.
Под действием специального фермента (ДНК-полимеразы) разрываются водородные связи
между нуклеотидами двух цепочек, и к связям, освободившиеся по принципу
комплементарности присоединяются соответствующие нуклеотиды ДНК (А-Т, Г-Ц). Следовательно,
порядок нуклеотидов в «старом» цепочке ДНК определяет порядок нуклеотидов в
«новому», то есть «старый» цепочка ДНК является матрицей для синтеза «нового». Такие
реакции называются реакциями
матричного синтеза, они характерны только для живого. Молекулы ДНК могут
содержать от 200 до 2x108 нуклеотидов. Огромное разнообразие
молекул ДНК достигается различными их размерами и разной последовательностью
нуклеотидов.
Роль ДНК в клетке заключается в хранении, воспроизведении и передаче
генетической информации. Благодаря матричному синтезу наследственная информация дочерних
клеток точно соответствует материнской.
РНК, как и ДНК, является полимером, построенным из мономеров - нуклеотидов.
Структура нуклеотидов РНК похожа с такой ДНК, но есть следующие отличия:
вместо дезоксирибози в состав нуклеотидов РНК входит пяти углеродный сахар
- рибоза, а вместо азотной основания тимина - урацил. Остальные трех азотных основ
те же: аденин, гуанин и цитозин. По сравнению с ДНК в состав РНК входит меньше
нуклеотидов и, следовательно, его молекулярная масса меньше.
Известны двух - и одноланцюжкові РНК. Дволанцюжкові РНК содержатся в некоторых
вирусах, что виконуть (как и ДНК) роль хранителя и передатчика наследственной
информации. В клетках других организмов встречаются одноланцюжкові РНК, которые являются
копиями соответствующих участков ДНК.
В клетках существуют три типа РНК: информационная, транспортная и
рибосомальна. Информационная РНК (и-РНК) состоит из 300-30 000 нуклеотидов и
составляет примерно 5 % от всей РНК, содержащейся в клетке. Она является копией
определенного участка ДНК (гена). Молекулы и-РНК выполняют роль переносчиков
генетической информации от ДНК к месту синтеза белка (рибосомы) и
непосредственно участвуют в сборе его молекул.
Транспортная РНК (т-РНК) составляет до 10 % от всей РНК клетки и
состоит из 75-85 нуклеотидов (рис. 129). Молекулы т-РНК транспортируют
аминокислоты из цитоплазмы в рибосомы.
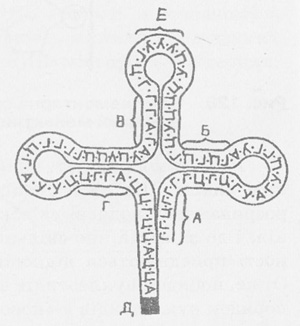
Рис. 129. Схема строения т-РНК. А, В, В,
Г - участки комплементарного соединения внутри одной цепочки РНК; Д - активный
центр (участок соединения с аминокислотой); Е - участок комплементарной соединения с
молекулы и РНК.
Основную часть РНК цитоплазмы
(около 85 %) составляет рибосомальна РНК (р-РНК). Она входит в состав
рибосом. Молекулы р-РНК включают 3-5 тыс.
нуклеотидов. Считают, что р-РНК
обеспечивает определенное пространственное взаиморасположение и-РНК и т-РНК.