РАЗДЕЛ II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
9. Неметаллические элементы и их соединения. Неметаллы
9.4. Элементы VA группы
9.4.4. Соли аммония
Соли аммония содержат в своем составе сложный катион NH4+. Это кристаллические вещества с йонним типом связи, имеют йонни кристаллические решетки, в узлах которых размещаются катионы (NH4+) и анионы (кислотные остатки). Ион NH4+ имеет тетраедричну строение и образуется по донорно-акцепторным механизмом таким образом:
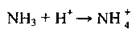
Ион аммония NH4+ проявляет свойства иона одновалентного металлического элемента.
Физические свойства солей аммония
Соли аммония - это преимущественно бесцветные1 кристаллические вещества, термически неустойчивы, хорошо растворимые в воде; в растворах диссоциируют полностью:
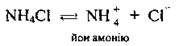
Добыча солей аммония
Взаимодействие аммиака NH3 с кислотами:
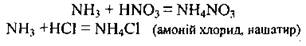
Химические свойства солей аммония
Как сильные электролиты соли аммония в водном растворе диссоциируют на ионы аммония и ионы кислотного остатка:
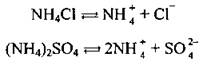
1. Соли аммония вступают в реакции ионного обмена:
а) со щелочами при нагревании (качественная реакция на ион аммония NH4+). Аммиак, выделяющийся распознают по запаху или по изменению цвета влажной лакмусовой бумажки:
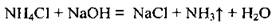
б) некоторые соли реагируют с кислотами:

в) с другими солями:
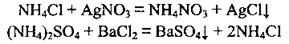
2. Термическое разложение солей аммония:
а) если соль аммония образована кислотой-неокисником, то она разлагается с образованием NH3:
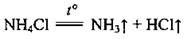
Это обратимая реакция; при нагревании равновесие смещается вправо, а на холоде - влево:
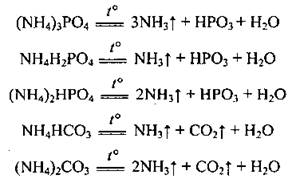
б) если кислота нелетка, то может быть частичное разложение:
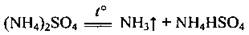
в) если анион кислоты проявляет окислительные свойства, то происходит необратимая реакция:
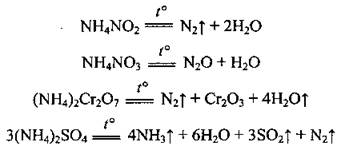
Применение солей аммония
1. Аммоний нитрат (аммиачная селитра) NH4NО3, аммоний сульфат (NH4)2SО4, аммоний дигідрогенортофосфат NH4H2PO4 и аммоний гідрогенортофосфат (NH4)2HPВ4 являются важными минеральными удобрениями.
2. Аммоний гідрогенкарбонат NH4HCВ3 (известный под бытовой названием амоняк) используют как разрыхлитель теста в кондитерском производстве (Е 503).
3. Аммоний хлорид (нашатырь) NH4Cl применяют в сухих гальванических элементах.
_____________________________________________________________
1 Аммоний дихромат (NH4)2Cr2О7 - соль оранжевого цвета, обусловленного окраской дихромат-иона.