РАЗДЕЛ II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
9. Неметаллические элементы и их соединения. Неметаллы
9.4. Элементы VA группы
9.4.1. Общая характеристика
В состав главной подгруппы V группы1 входят Азот N, Фосфор Р, Мышьяк As, Стибій Sb и Висмут Ви.
Строение внешнего электронного слоя элементов - ns'2np3. Это p-элементы:
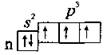
Валентность Азота - III, а у остальных элементов - III и V. Как элемента 2-го периода, в атома Азота нет d-подуровня, поэтому возбуждение атома невозможно. Именно по этой причине Азот никогда не проявляет валентности V. У остальных элементов VA группы во время возбуждения атома возможен переход спаренных электронов на вакантные d-орбитали (n ≥ 3):
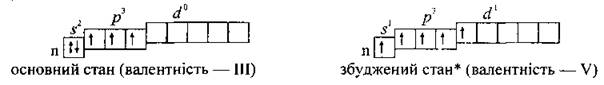
Атом Азота, кроме трех ковалентных связей может образовывать еще один связь по донорно-акцепторный механизм, то есть предоставлять свою неразделенную пару электронов на свободную орбиталь атома другого элемента. Таким образом, максимальная валентность Азота - IV.
В соединениях элементы группы Азота, кроме Стиба и Висмута, могут проявлять самую низкую степень окисления (-3). Все элементы подгруппы способны проявлять также и положительные степени окисления - +3 и +5.
В группе от Азота до Висмута возрастает радиус атома, ослабляется притяжение валентных электронов к ядру, а поэтому уменьшается электроотрицательности, неметаллические свойства элементов и увеличиваются металлические. Бисмут уже принадлежит к металлических элементов.
Общая формула гідрогеновмісних соединений - ЭН3. Это аммиак (нашатырный спирт) NH3, фосфин РН3, арсиное AsH3, стибін SbH3, вісмутин Он3. Степень окисления Азота в этих соединениях - -3, поэтому для них характерны восстановительные свойства.
Общие формулы оксидов элементов группы - Е2О3 и E2O5. Они имеют кислотный характер, поэтому им соответствуют кислоты Н3ЭО3 и Н3ЭО4. Кислотные свойства оксидов в ряду N2О5 - Р2О5 -As2О5 - Sb2Е5 - Е2О5 ослабляются.
______________________________________________________________
1 По новой номенклатуре - 15 группы.