РАЗДЕЛ II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
9. Неметаллические элементы и их соединения. Неметаллы
9.3. Элементы VIA группы
9.3.4. Озон
Озон O3 - это еще одна алотропна модификация Кислорода. Относительная молекулярная масса - 48, молярная масса - 48 г/моль. Это газ со своеобразным, резким «металлическим» запахом, очень ядовит. Озон - более сильный окислитель, чем кислород.
Распространенность в природе
Около 90% природного озона находится в стратосфере на высоте 12-50 км (максимальная плотность - на высоте 20-25 км1), образуя так называемый озоновый слой. Понятно, что там он существует в чрезвычайно разреженном состоянии: если бы весь озон привести в нормальных условиях (н. у.), то образовался бы слой, толщина которого была бы примерно 3 мм2. Он поглощает львиную долю ультрафиолетового солнечного излучения (длина волны - 175-242 нм), которое является опасным для всего живого. Причем ультрафиолет поглощается и в процессе образования озона (во время образования атомарного Кислорода3):
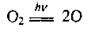
и во время его разложения, фотолізу:
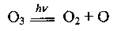
Еще 10% атмосферного озона содержит тропосфера - нижний слой атмосферы, который достигает 10-12 км (в умеренных широтах), и особенно низкий, приземный слой (смоговий озон), наибольшая концентрация которого наблюдается над городами (так как он образуется при электрическом разряде). Вследствие токсического действия имеет негативное влияние на живые объекты.
Есть озон и в хвойных лесах (7 · 10-6 %), где он образуется в результате окисления смолистых веществ.
Свойства озона
Озон - неустойчивое вещество. При его разложении образуется атомарный Кислород, что обуславливает высокую окислительную активность озона. Озон не окисляет только золота Аu, платины Pt и иридия Иr.
С некоторыми металлами озон образует озониды:
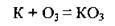
Качественная реакция на озон
Озон не окисляет хлорид - и бромид-ионов, однако окисляет іодид-ионы:
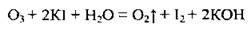
Добывания озона
В лаборатории озон получают из кислорода (или воздуха) с помощью озонатора под действием «тихих» (без искры) электрических разрядов:
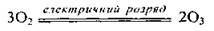
В природе озон образуется во время грозы, а в стратосфере под действием ультрафиолета солнечного излучения.
Применение озона
1. Обеззараживания воздуха и питьевой воды (озонирование - процесс менее вреден, чем хлорирование).
2. Дезинфекция помещений4, одежды, стерилизация перевязочного материала в медицине.
3. Отбеливание бумаги.
4. Получение различных веществ в химической промышленности и в лаборатории (камфоры, ванилина, моно - и дикарбоновых кислот).
5. Озонирование сточных вод химических предприятий (прежде всего в случае фенольных и цианидным загрязнений).
______________________________________________________________
1 Здесь его концентрация циклически колеблется в соответствии с 11-летнего цикла активности Солнца.
2 Как уже упоминалось, вся атмосфера, толщина которой достигает 100 км, приведенный к н. у., была бы толщиной 8 км.
3 в Дальнейшем он присоединяется к молекуле кислорода, образуя молекулу озона.
4 При использовании бактерицидной УФ-лампы микроорганизмы погибают не только непосредственно под действием ультрафиолетового излучения, но и вследствие действия озона, который образуется в помещении во время работы такой лампы.
Предостережение (!): такие лампы нельзя использовать для загара, смотреть на них (во время работы).