ЗАКОНЫ СОХРАНЕНИЯ. СТЕХИОМЕТРИИ
В химических реакциях атомы не
образуются заново и не разрушаются. Этот факт отражают законы стехиометрии.
Масса веществ, вступивших в химическую
реакцию, равна массе веществ, образовавшихся в результате реакции (закон
сохранения массы).
Объемы газов, что реагируют,
относятся друг к другу и к объему полученных газов как простые целые числа
(закон объемных отношений). Равные объемы газов при одинаковых температуре и давлении
содержат одинаковое количество молекул (с а к о
н Авогадро).
НЕКОТОРЫЕ ФИЗИЧЕСКИЕ ВЕЛИЧИНЫ И ИХ ЕДИНИЦЫ
В табл.1 приведены физические величины,
которые чаще всего используют в химии.
Таблица 1
Некоторые физические величины и их единицы
|
Физическая величина
|
Символ
|
Единица измерения
физической величины
|
Обозначения
|
|
украинское
|
международное
|
|
Количество
вещества В
|
n(В), ν
|
Моль
|
моль
|
mol
|
|
Масса
|
m
|
Килограмм
|
кг
|
kg
|
|
Молярная масса
вещества В
|
М( В)
|
Грамм на моль
|
г/моль
|
g/mol
|
|
Объем
|
V
|
Кубический метр, литр (10-3 м3)
|
м3, л
|
m3, L
|
|
Молярный объем
|
Vn
|
Литр на моль
|
л/моль
|
L/mоl
|
|
Температура
|
Т
|
Кельвин
|
К
|
K
|
|
Температура
|
t
|
Градус Цельсия
|
°С
|
°С
|
|
Давление
|
г
|
Паскаль
|
Па
|
Ра
|
|
Количество теплоты
|
Q
|
Джоуль
|
Дж
|
J
|
|
Энергия
|
Е
|
Джоуль
|
Дж
|
J
|
Моль - единица количества вещества.
Моль - это такое количество вещества,
которая содержит столько молекул, атомов или ионов, сколько атомов содержится в
ізотопі Карбона массой 0,012 кг.
В 1 моль Углерода содержится 6,02 • 1023 атомов. Это число называется постоянной
Авогадро
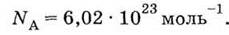
Количество вещества n(В) можно вычислить по формулам:
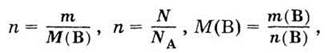
где
m - масса вещества; М(В) - молярная
масса вещества; N - число частиц в веществе.