ПРОВЕРЬ СВОИ ЗНАНИЯ
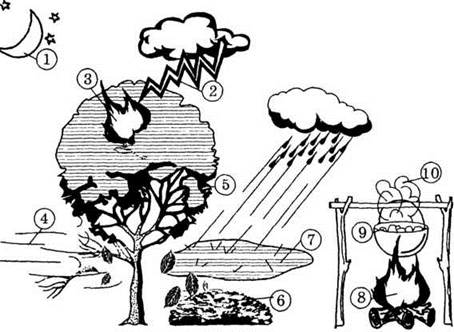
ПРЕДМЕТ ХИМИИ
Какие физические и химические явления и
процессы обозначены цифрами?
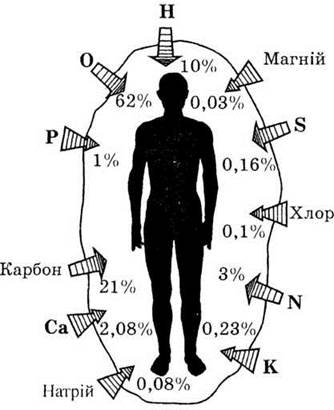
ХИМИЧЕСКИЙ ЭЛЕМЕНТ
Назовите химические элементы, обозначенные
символами, или запишите символы названных элементов, процентное содержание которых в
организме человека указано на рисунке.
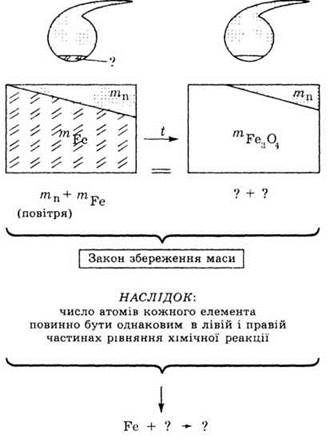
КОЛИЧЕСТВЕННЫЕ СООТНОШЕНИЯ В ХИМИИ
Объясните опыт М. В. Ломоносова
(1748 г.) и напишите
уравнение реакции, которое произошло в этом опыте.
КИСЛОРОД
1. Заполните схему, написав
формулы конкретных веществ.
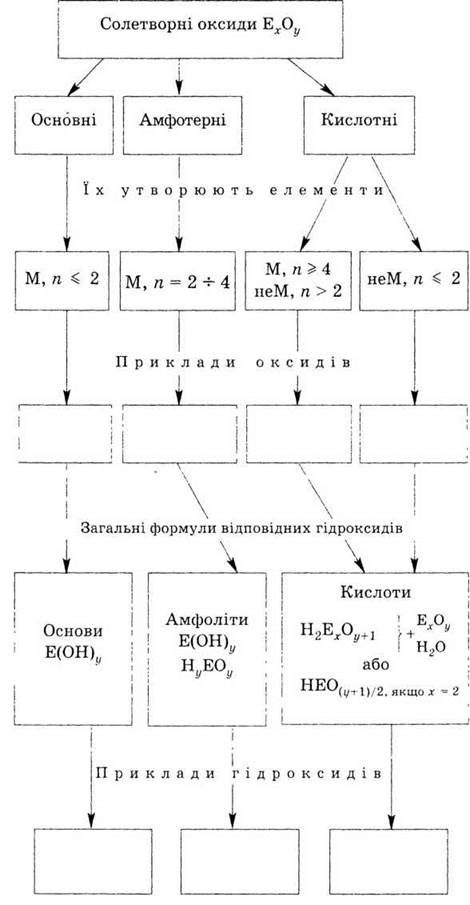
Обозначения: Э - химический элемент, М
- металл, неМ - неметал, n - валентность.
2. Используя схему «Химические
свойства кислорода», напишите уравнения соответствующих реакций
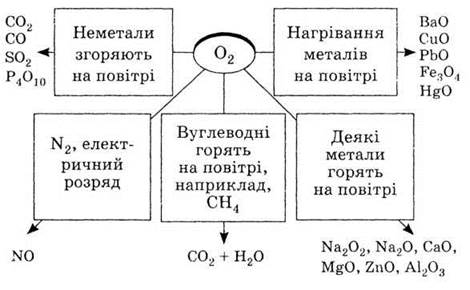
3. Напишите уравнения реакций, которые
соответствуют схеме, укажите условия их проведения
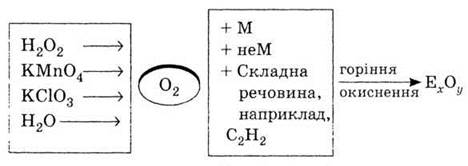
ВОДОРОД
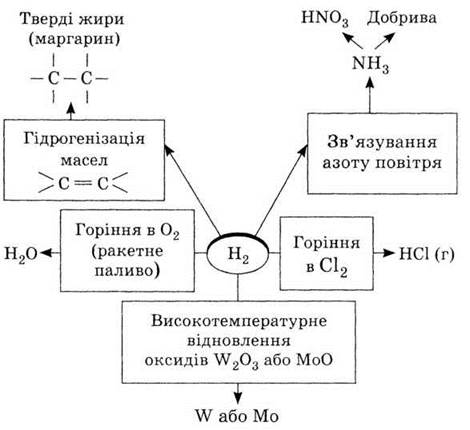
Используя схему «Применение
водорода в промышленности», напишите уравнения соответствующих реакций
ВОДА. ВОДНЫЕ РАСТВОРЫ
Напишите химические формулы и уравнения
реакций к схеме «Химические свойства воды»
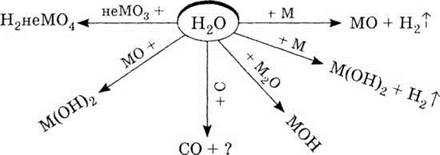
Обозначения: М - металл, неМ -
неметал.
ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
1. Конкретизируйте схему «Классификация
неорганических веществ», записав формулы веществ
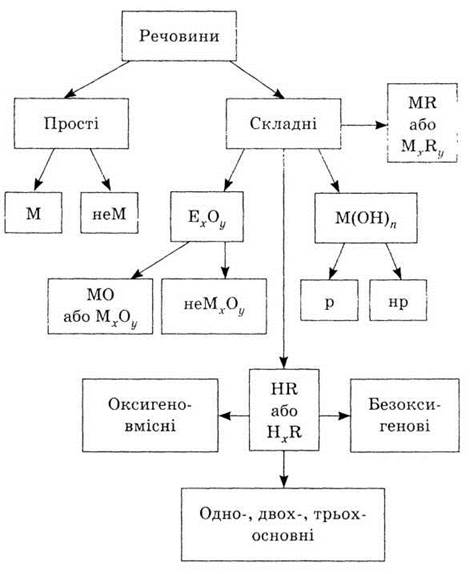
Обозначения: Э - химический элемент, М
- металл, неМ - неметал, R - кислотный остаток, р - растворимые,
нр - нерастворимые.
2. Конкретизируйте схему «Оксиды и их
химические свойства», записав формулы веществ и соответствующие уравнения реакций.
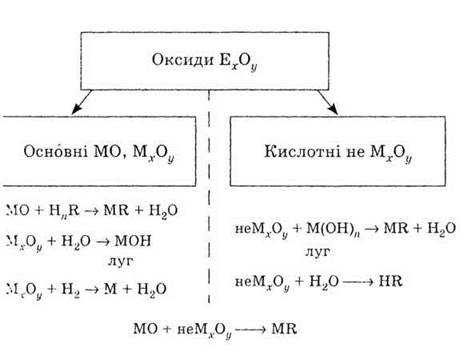
Обозначения: Э - химический элемент, М
- металл, неМ - неметал, R - кислотный остаток.
3. Конкретизируйте схему «Кислоты и
их химические свойства», записав формулы веществ и соответствующие уравнения
реакций. Укажите окраски индикаторов в растворе кислот.
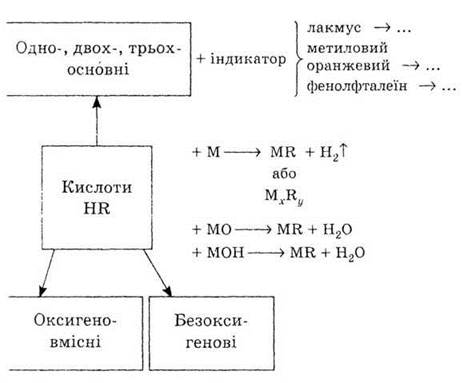
Обозначения: М - металл, R - кислотный остаток.
4. Дополните и конкретизируйте схему
«Состав и химические свойства кислот».
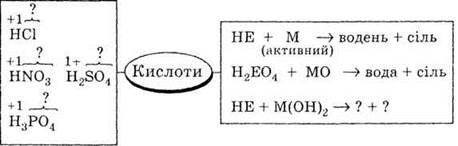
Обозначения: Э - химический элемент, М
- металл.
5. Конкретизируйте схему «Генетический
связь классов неорганических веществ», записав формулы веществ.
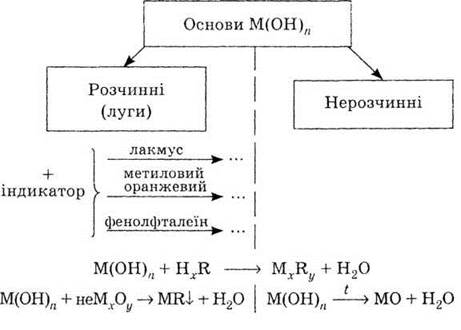
Обозначения: М - металл, неМ -
неметал, R - кислотный остаток.
6. Конкретизируйте схему «Генетический
связь классов неорганических веществ», записав формулы веществ.
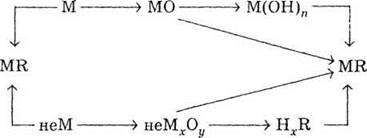
Обозначения: М - металл, неМ -
неметал, R - кислотный остаток.
7. Конкретизируйте схему химических
преобразований, записав формулы веществ и соответствующие уравнения реакций.
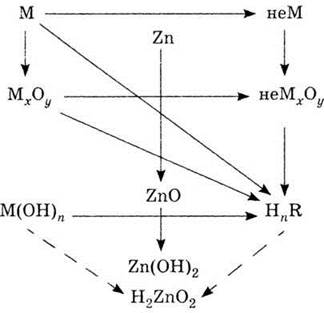
Обозначения: М - металл, неМ -
неметал, R - кислотный остаток.
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
Заполните таблицу на основе данных,
приведенные в первой графе.
|
Общая схема
уравнение химической реакции
|
A+B →
AB
|
1) AB → A+B
2) ABC → A+B+C
|
AB+C → A+CB
|
AB+CD → CB+AD
|
|
Тип химической
реакции
|
|
|
|
|
|
Примеры уравнений
химической реакции
|
|
|
|
|
СТРОЕНИЕ АТОМА
Классифицируйте вещества, исходя из
типа химической связи в них:
СН4, KCl, CS2, Н2, F2, S8, HBr,
CaO, Н2O, CaF2, CH3Cl, РН3, Аl2O3
ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА
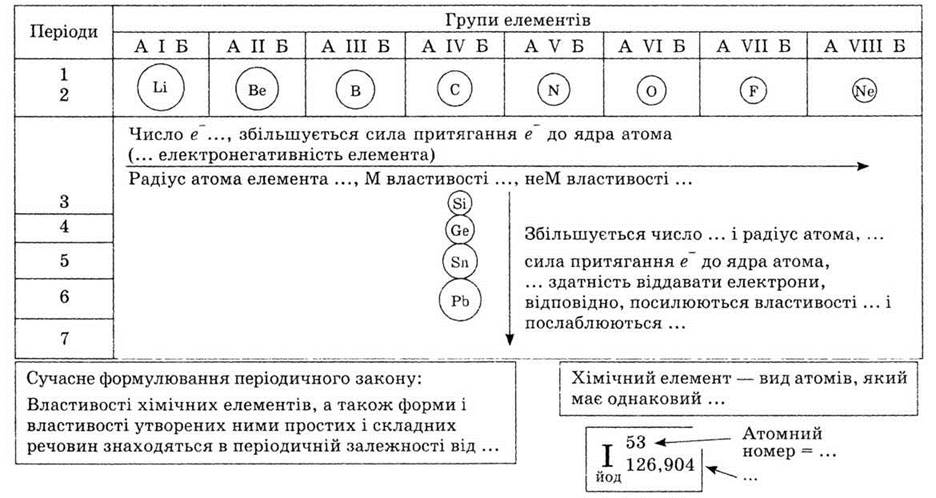
Вставьте пропущенные слова в текст
схемы, которая отражает строение периодической системы химических элементов Д. И. Менделеева и периодичность изменения их свойств.
Номер
периода = ...
Номер группы
= ... на внешнем
энергетическом уровне
атома
ГАЛОГЕНЫ
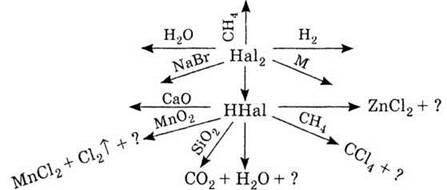
1. Используя схему
«Преобразования галогенов (l) и их соединений», напишите уравнения
соответствующих реакций.
2. Напишите уравнения реакций, которые
соответствуют преобразованиям:
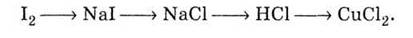
ЩЕЛОЧНЫЕ МЕТАЛЛЫ
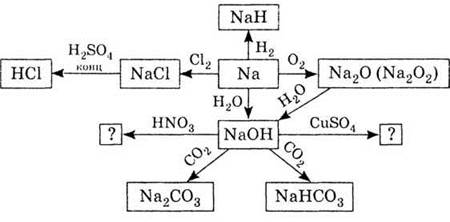
Используя схему «Преобразования
натрия и его соединений», напишите уравнения соответствующих реакций.
ЭЛЕКТРОЛИТЫ
Используя диаграмму, напишите
уравнения диссоциации для конкретных веществ 1-6 и формулы веществ-неэлектролита
7-10.
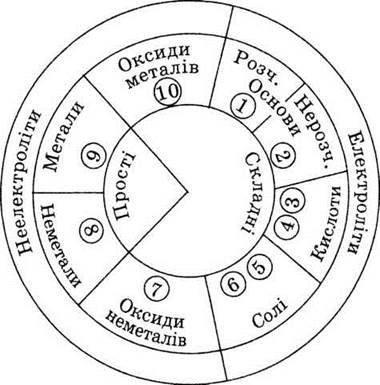
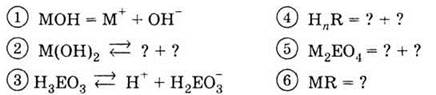
Обозначения: Э - химический элемент, М
- металлический элемент, R - кислотный остаток.
ОТ НАТРИЯ ДО АРГОНА
Заполните таблицу, обобщая
сведения о высшие оксиды и гидроксиды химических элементов 3-го периода
периодической системы Д. И. Менделеева.
|
Символ
|
23 11Na
|
24 12Mg
|
27 13Al
|
28 14Si
|
31 15P
|
32 18S
|
35 17Cl
|
40 18Ar
|
|
Электронная формула внешнего
энергетического уровня
|
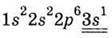
|
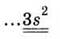
|
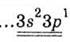
|
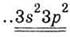
|
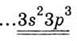
|
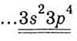
|
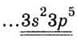
|
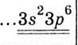
|
|
Формула высшего оксида
|
|
|
|
|
|
|
|
|
|
Характер химических свойств
высшего оксида
|
|
|
|
|
|
|
|
|
|
Формула гидроксида
|
|
|
|
|
|
|
|
|
|
Характер химических свойств
гидроксида
|
|
|
|
|
|
|
|
|
ХИМИЯ НЕМЕТАЛЛИЧЕСКИХ ЭЛЕМЕНТОВ
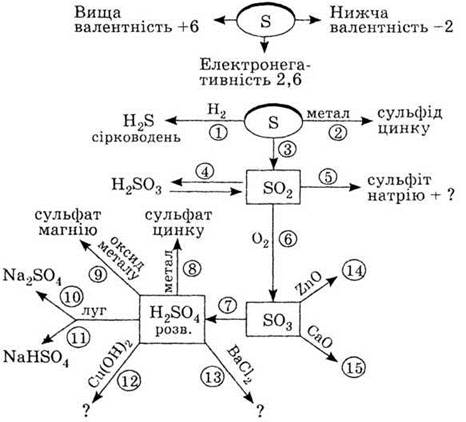
1. Используя схему «Сера и ее
соединения», напишите молекулярные уравнения реакций 1, 2, 3, 6, 7, 8, 14, 15, полные
и сокращенные ионные уравнения реакций 5, 9, 10, 11, 12, 13. Объясните
окислительно-восстановительный процесс, который соответствует уравнениям реакций 1, 2, 8.
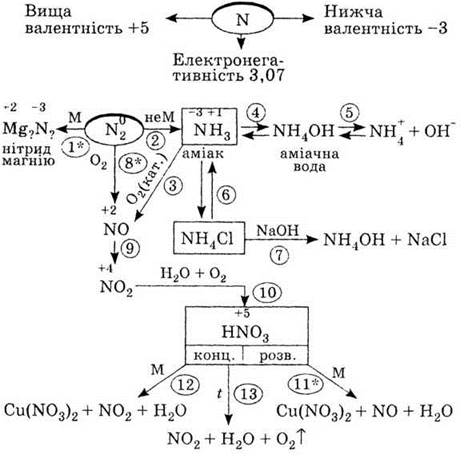
2. Используя схему «Азот и его
соединения», напишите уравнения реакций (1-13). Объясните окислительно-восстановительные процессы,
обозначены звездочкой.
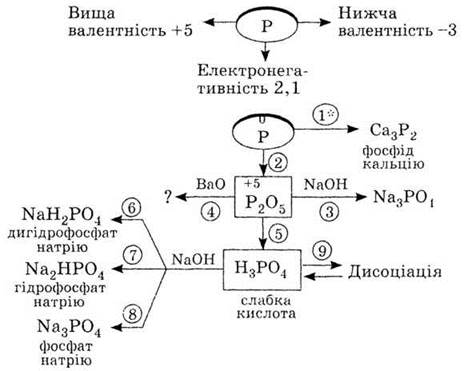
3. Используя схему «Фосфор и
его соединения», напишите уравнения реакций 1-9. Объясните окислительно-восстановительные процессы,
обозначены звездочкой.
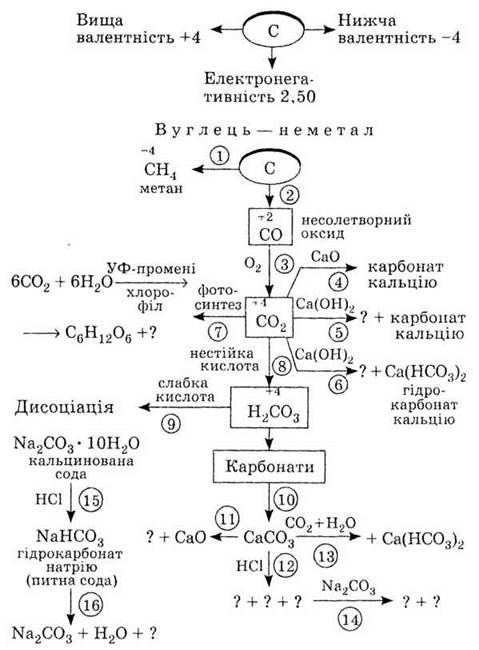
4. Используя схему «Углерод и
его соединения», напишите уравнения реакций 1-16.
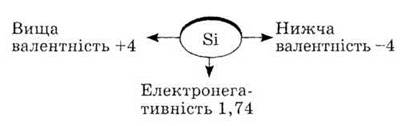
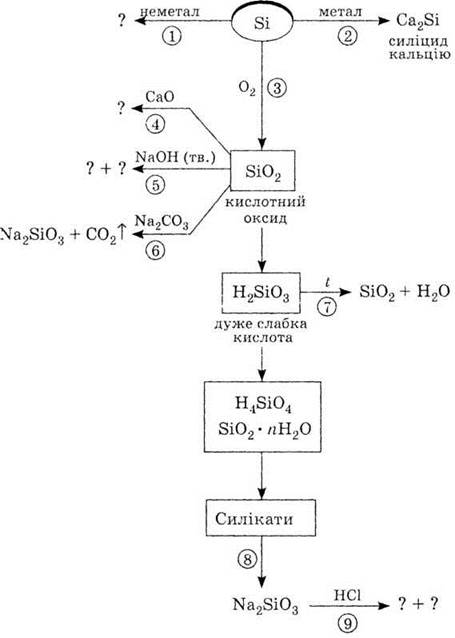
5. Используя схему «Кремний и
его соединения», напишите уравнения реакций 1-9.
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
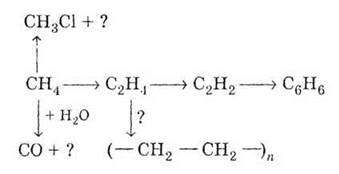
Напишите уравнения реакций, которые
соответствуют следующим преобразованием:
ХИМИЯ МЕТАЛЛИЧЕСКИХ ЭЛЕМЕНТОВ
1. Используя схему «Общие
химические свойства металлов», напишите уравнения реакций 1-8. Объясните
окислительно-восстановительные процессы, отмеченные звездочкой.
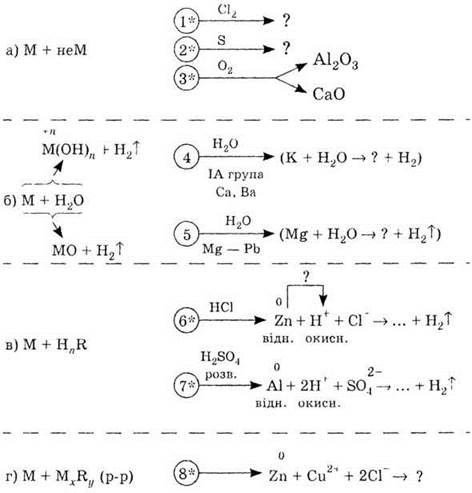
Обозначения: М - металл, неМ -
неметал, R -
кислотный остаток.
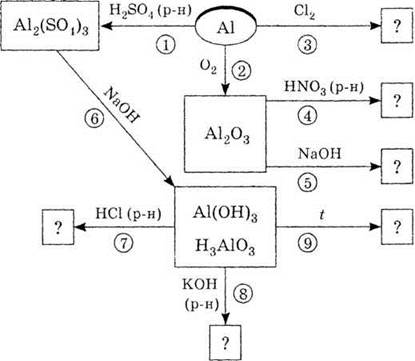
2. Используя схему «Алюминий и
его соединения», напишите уравнения реакций 1-9.
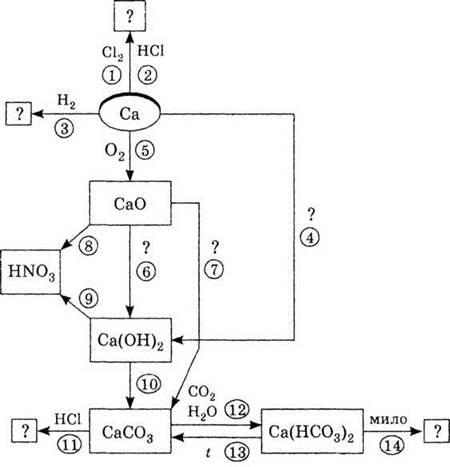
3. Используя схему «Кальций и
его соединения», напишите уравнения реакций 1-14.
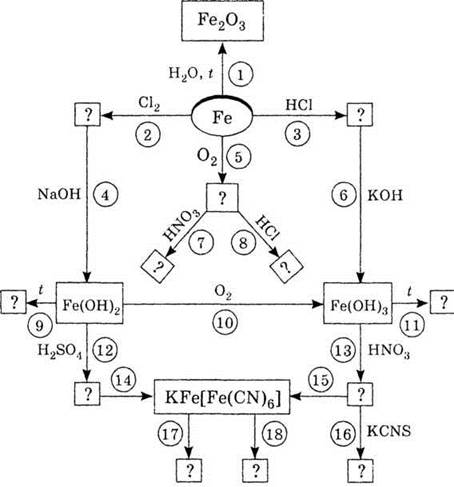
4. Используя схему «Железо и
его соединения», напишите уравнения реакций 1-18.
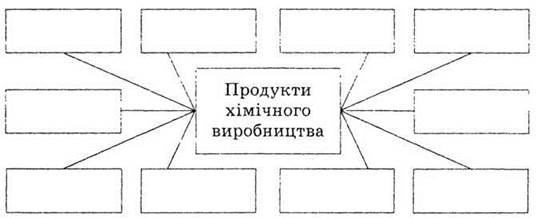
ОБОБЩАЮЩАЯ СХЕМА КРАТКОГО КУРСА
Приведите примеры применения
продуктов химического производства.