ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОРГАНИЧЕСКАЯ
ХИМИЯ
ОБЩАЯ
ХАРАКТЕРИСТИКА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Брутто, структурные и электронные
формулы соединений
Второй
постулат Вутлерова. Химические реакционные способности определенных групп атомов существенно зависят
от их химического окружения, то есть от того, с какими атомами или группами
атомов соседствует определенная группа.
Формулы
соединений, которыми мы пользовались при изучении неорганической химии, отражают
только количество атомов того или иного элемента в молекуле. Такие формулы
называют «брутто - формулами», или «молекулярными формулами».
Как
вытекает из первого постулата Вутлерова, в органической химии важна не только
количество тех или иных атомов в молекуле, а еще и порядок их связывания,
то есть брутто-формулы не всегда целесообразно использовать для органических соединений.
Например, для наглядности при рассмотрении структуры молекулы метана мы
использовали структурные формулы - схематическое изображение порядка связывания
атомов в молекулу. При изображении структурных формул химическая связь обозначают
чертой, двойная связь - двумя черточками и т.д.
Электронная
формула (или формула Льюиса) очень похожа на структурную формулу, но в этом случае
изображают не образованные связи, а электроны, как те, что образуют связь, так и
те, что его не образуют.
Например,
уже рассмотренную сульфатную кислоту можно записать с помощью следующих формул.
Брутто-формула - Н2804, структурная и электронная формулы
имеют такой вид:

Структурные
формулы
органических соединений
Почти
все органические вещества состоят из молекул, состав которых выражается химическими
формулами, например СН4, С4Н10, С2Н4О2.
А какое строение имеют молекулы органических веществ? Этот вопрос задавали себе в
середине XIX века основатели органической химии - Ф. Кекуле и А. М. Вутлеров.
Исследуя состав и свойства различных органических веществ, они пришли к
следующих выводов:
- атомы в молекулах органических веществ соединены
химическими связями в определенной последовательности, согласно их валентности. Эту
последовательность принято называть химическим строением;
- атомы Углерода во всех органических соединениях
чотиривалентні, а другие элементы проявляют характерные для них валентности.
Эти
положение является основой теории строения органических соединений, сформулированной О. М.
Бутлеровим в 1861 году.
Химическую
строение органических соединений наглядно подают структурными формулами, в которых химические
связи между атомами обозначают черточками. Общее число черточек, отходящих от
символа каждого элемента, равна его валентности атома. Кратные связи
изображают двумя или тремя черточками.
На
примере насыщенного углеводорода пропана С3Н8 рассмотрим,
как составить структурную формулу органического вещества.
1. Изображаем карбоновый скелет. В данном случае
цепь состоит из трех атомов Углерода:
С-С-С
2. Карбон четырехвалентное, поэтому от каждого атома
Карбона изображаем недостаточные черты таким образом, чтобы рядом с каждым атомом было
по четыре черты:
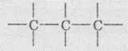
3.
Дописываем символы атомов Водорода:
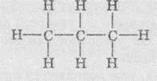
Часто
структурные формулы записывают в сокращенном виде, не изображая связи С -
Н. Сокращенные структурные формулы гораздо компактнее, чем развернутые:
СН3
- СН2 - СН3.
Структурные
формулы показывают только последовательность соединения атомов, но не отображают
пространственного строения молекул, в частности валентные углы. Известно, например, что угол
между связями С в пропане равен 109,5°. Однако структурная формула пропана
выглядит так, будто этот угол равен 180°. Поэтому правильнее было бы записывать
структурную формулу пропана в менее удобном, но в более истинном виде:
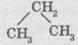
Профессиональные
химики используют следующие структурные формулы, в которых вообще не показаны ни
атомы Карбона, ни атомы Водорода, а изображен только карбоновый скелет в
виде соединенных между собой С-С-связей, а также функциональные группы. Для
того чтобы костяк не выглядел одной сплошной линией, химические связи изображают
под углом друг к другу. Так, в молекуле пропана С3Н8
всего две связи С-С, поэтому пропан изображают двумя черточками.
Гомологические ряды органических соединений
Рассмотрим
структурные формулы двух соединений одного класса, например спиртов:
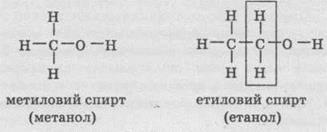
Молекулы
метилового СН3ОН и этилового С2Н5ОН спиртов
имеют одинаковую функциональную группу ОН, общую для всего класса спиртов, но
отличаются длиной карбонового скелета: в этаноле на один атом Углерода
больше. Сравнивая структурные формулы, можно заметить, что при увеличении
карбонового цепи на один атом Углерода состав вещества меняется на группу СН2,
при удлинении карбонового цепи на два атома - на две группы СН2
т.д.
Соединения
одного класса, имеющих подобное строение, но отличающиеся по составу на одну или
несколько групп СН2, называют гомологами.
Группу
СН2 называют гомологической разностью. Совокупность всех гомологов
образует гомологический ряд. Метанол и этанол относятся к гомологическому ряду
спиртов. Все вещества одного ряда имеют сходные химические свойства, а их
состав можно выразить общей формулой. Например, общая формула
гомологического ряда спиртов - СnН2n+1ВОН, где n - натуральное число.
|
Класс
соединений
|
Общая формула
|
Общая
формула с выделением функциональной группы
|
|
Алканы
|
СnН2n+2
|
|
|
Циклоалкани
|
СnН2n
|
|
|
Алкены
|
СnН2n
|
|
|
Алкадієни
|
СnН2n-2
|
|
|
Алкіни
|
СnН2n-2
|
|
|
Одноядерные арены (гомологический ряд
бензену)
|
СnН2n-6
|
|
|
Одноатомные спирты насинені
|
СnН2n+2В
|
СnН2n+1ВH
|
|
Многоатомные спирты
|
СnН2n+2Оx
|
СnН2n+2-x(ВH)x
|
|
Альдегиды
|
СnН2nВ
|
СnН2n+1CHO
|
|
Одноосновны карбоновые кислоты
|
СnН2nО2
|
СnН2n+1COOH
|
|
Эстеры
|
СnН2nВ
|
СnН2n+1COOCnH2n+1
|
|
Углеводы
|
Сn(Н2О)m
|
|
|
Амины первичные
|
СnН2n+3N
|
СnН2n+1NH2
|
|
Аминокислоты
|
СnН2n+1NO
|
Н2NCnH2nCOOH
|