ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОРГАНИЧЕСКАЯ
ХИМИЯ
ОБЩАЯ
ХАРАКТЕРИСТИКА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Химическая структура и химическая
строение
Первый
постулат Бутлерова. В молекулах веществ существует определенный порядок связывания атомов,
что называется химической структурой или строением вещества.
Каждой
индивидуальной веществу соответствует одна-единственная определенная химическая структура.
В
органической химии Карбон всегда находится в чотиривалентному состоянии, то есть может
образовывать максимум четыре химические связи.
Рассмотрим
строение молекулы метана СН4. В этом соединении степень окисления атома
Углерода равна -4, а атомов Водорода 4-1. В пространстве атомы Водорода могут
находиться в такой способ: или в плоскости в вершинах квадрата, или в вершинах
треугольной пирамиды, так называемого тетраэдра. Это можно проиллюстрировать с помощью
структурных формул, в которых связи между атомами обозначают черточками:

Однако
форма квадрата невозможна, потому что из-за отталкивания атомов Водорода один
от одного будет происходить деформация структуры, и напоследок молекула достигнет
состояния, в котором атомы Водорода находятся в вершинах тетраэдра. При
рентгеноструктурному анализу метана было выяснено, что длина связей С-Н
равен 0,11 нанометров (1 нм равен 10-9 метра), а с точки зрения
стереометрии было выяснено, что угол  НСН равна 109,28°.
НСН равна 109,28°.
Следовательно,
наглядно строение молекулы метана можно представить так:
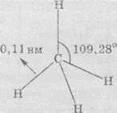
В
принципе, и в более сложных органических молекулах, в которых атомы Водорода
замещенные различными заместителями, углы и длины связей будут стремиться к
приведенных выше значений, то есть цепочка атомов Карбона (длина С-С связи
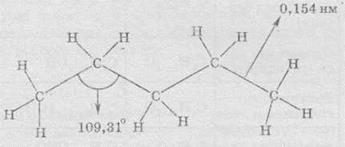
равна 0,164 нм) будет не линейным, а зигзагообразным, с углом  ССС, который примерно равен 110°. Например, строение молекулы
пентана С5Н12 можно представить так:
ССС, который примерно равен 110°. Например, строение молекулы
пентана С5Н12 можно представить так: