ХИМИЯ МЕТАЛЛИЧЕСКИХ ЭЛЕМЕНТОВ
АЛЮМИНИЙ
Алюминий - третий по распространенности
элемент земной коры. Он входит в состав многих силикатных минералов, которые
называются алюмосилікатами. Важнейшим природным соединением алюминия, что
стала сырьем для производства металла, является боксит 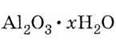 - гидратований оксид алюминия.
- гидратований оксид алюминия.
Алюминий - очень активный металл. В
ряду активности металлов стоит левее многих других металлов, поэтому
используется для промышленного получения некоторых редких металлов путем
восстановление их оксидов металлическим алюминием при высокой температуре, например:
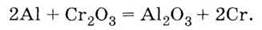
Метод получения металлов из их оксидов
с помощью алюминия называется алюмінотермією. Важнейшее соединение Алюминия
- оксид Аl2О3. Он обладает
амфотерністю, что проявляется во взаимодействии его и с кислотами, и с основаниями:
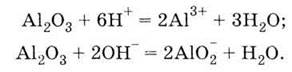
Алюминий получают разложением электрическим
током раствора его оксида в раз плавленом криолите СNaF •
АlF3:
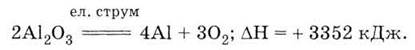
Через высокую энергию химического
связи в оксиде алюминия процесс его разложения чрезвычайно энергоемкий, что
ограничивает использование алюминия.
Таблица
Алюминий и его соединения
|
Алюминий
|
Соединения Алюминия
|
|
оксид алюминия
|
гидроксид алюминия
|
|
1. Серебристо-белый
легкий металл
2. Окисляется
на воздухе с образованием защитной оксидной пленки:
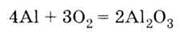
3. Вытесняет
водород из воды:
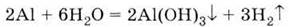
4. Взаимодействует
с кислотами:
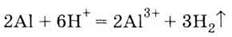
5. Взаимодействует
с щелочами:
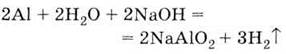
6. Вытесняет
металлы из их оксидов (алюмінотермія):
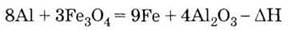
Получение
Расписание
электрическим током расплава оксида алюминия (в криолите):
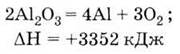
|
1. Очень
твердый порошок белого цвета
2. Амфотерный
гидроксид взаимодействует:
с
кислотами
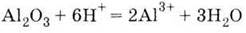
с щелочами:
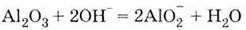
Образование
а) при
окислении или горении алюминия на воздухе:
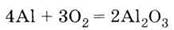
б) в
процессе алюмінотермії:
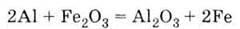
в) при
термическом разложении гидроксида алюминия:
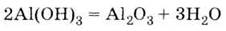
|
1. Белый
нерастворимый в воде порошок
2. Проявляет
амфотерные свойства, взаимодействует:
с
кислотами:
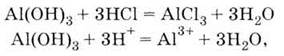
с щелочами:
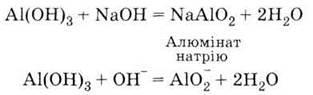
3. Раскладывается
при нагревании:
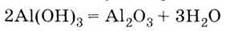
Образование
а) при
взаимодействия растворов солей алюминия с растворами щелочей (без избытка):
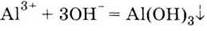
б) при
взаимодействия алюминатов с кислотами (без избытка):
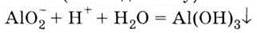
Соли
алюминия в водных растворах гидролизуются:
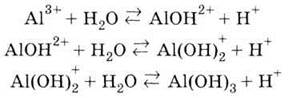
|
Однако и сам алюминий и его сплавы
широко применяются в промышленности, и масштабы применения этого металла
постоянно растут. Это обусловлено рядом факторов. Перечислим важнейшие из
них.
1. Алюминий - самый распространенный металл
земной коры. Его ресурсы практически неисчерпаемы.
2. Алюминий имеет высокую коррозионную
устойчивость, и изделия из него практически не требуют специальной защиты.
3. Небольшая плотность алюминия (2,7
г/см3) в сочетании с высокой прочностью и пластичностью его сплавов
делает алюминий незаменимым конструкционным материалом в самолетостроении и способствует
расширению его применения в наземном и водном транспорте, а также в
строительстве.
4. Относительно высокая
электропроводность алюминия позволяет заменять им в электротехнике значительно
дорогую медь.
5. Высокая химическая активность
алюминия используется в алюмінотермії.
6. Прочность химической связи в
оксиде А12O3 предопределяет его механическую прочность,
твердость. Природный оксид алюминия, корунд, - один из основных абразивных
материалов. Искусственный рубин - оксид алюминия с примесью хрома (для предоставления
расцветка) являются обязательными деталями механических часов (оси и подшипники;
чем больше «камней» в часах, тем они лучше).
Химические свойства алюминия и его
соединений приведены в таблице, приведенной выше.