ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОСНОВНЫЕ ЗАКОНЫ И ПОНЯТИЯ ХИМИИ
Основные количественные законы химии
Закон постоянства газа
Каждая
чистое вещество независимо от места и способа ее добывания имеет постоянный состав.
Например,
вода состоит из атомов Водорода и Кислорода, причем массовая доля атомов
Водорода в воде составляет 11,1%, а Кислорода - 88,9%. И независимо от места
добычи чистая вода - речная, дождевая или морская, полученная из Арктического или
Антарктического льда,- будет иметь одинаковый качественный и количественный состав.
Закон
постоянства состава сформулировал в 1799 году французский ученый Жозеф Луи Пруст.
Свое открытие Пруст сделал, опираясь на результаты количественного анализа
оксидов, сульфидов и хлоридов металлов. В результате проведенного весового анализа
оксигенових соединений Железа, Купруму, Олова, Меркурию и Свинца он
установил, что металлы, которые соответствуют этим элементам (железо, медь, олово,
ртуть, свинец), соединяются с кислородом всегда в одинаковых пропорциях. В этих же
работах он показал, что природный купрум карбонат и купрум карбонат, полученный
химиком в лаборатории, имеют тот же постоянный состав и цвет. Так же ничем не
отличается купрум оксид, полученный из малахита и полученный в результате
взаимодействия меди с кислородом.
Противоположных
взглядов придерживался его соотечественник Клод Бертолле, который утверждал, что
состав химических соединений может изменяться в зависимости от условий их добычи. Он
доказывал, что на прохождение химических реакций влияет масса, связь, летучесть,
растворимость, упругость и т.д. Началась научная полемика, которая продолжалась несколько
лет.
В
то же время в полемике принял участие английский ученый Джон Дальтон. Он тщательно
проанализировал массы веществ, вступающих в реакцию, на основании чего
сформулировал закон кратных отношений. После убедительных доказательств Пруста и
Дальтона взгляды Пруста были поддержаны лучшими химиками того времени, а позиции
Бертолле признаны ошибочными. Закон постоянства состава позволил установить
количественные соотношения атомов химических элементов в соединениях и стал основой определения
атомных масс элементов. Сейчас закон постоянства состава воспринимают как обычную вещь,
однако в то время открытие этого закона было прорывом в развитии химии как науки и
стало одним из существенных доказательств атомно-молекулярного учения.
Однако
идеи Бертолле получили новое толкование в XX веке, когда были открыты
многочисленные соединения переменного состава, к которым принадлежали некоторые оксиды, сульфиды,
нитриды и т.д. После этого открытия по предложению российского химика М.С.
Курнакова соединения с постоянным составом были названы дальтонідами, а с переменным -
бертолідами. Состав дальтонідів выражают с помощью простых формул
целочисленными индексами, например: Н2О, SО2,
С2Нб. А состав бертолідів меняется и не соответствует
стехиометрическим соотношением. Например, состав ванадий(II) оксида обычно
выражают с помощью формулы VВ, хотя
на самом деле его состав может изменяться в пределах от VO0,9 до VO1,3.
При взаимодействии циркония с азотом образуется цирконий нитрид. Кроме состава ZrN, являются нитриды ZrN0,59, ZrN0,69, ZrN0,74, ZrN0,89.
В
связи с наличием соединений переменного состава в современное формулировка закона
постоянства состава следует внести уточнение: состав соединений молекулярной структуры является
постоянным независимо от способа добывания; состав соединений со структурой немолекулярною
(атомной, ионной или металлической решеткой) не является постоянным и зависит от условий
добывания.
Закон
кратных соотношений
В
в 1803 году английский ученый Джон Дальтон на основании своих исследований сформулировал
закон простых кратных отношений: если два элемента образуют друг с другом
несколько химических соединений разного состава, то количества их составляющих меняются
дискретно и на ту же массу одного из них приходятся такие массы другого, которые
соотносятся между собой, как простые целые числа.
Сегодня
мы можем записать эти отношения как 1 : 1; 2 : 3; 1 : 2; 2 : 5 т.д. Например,
Карбон и Кислород образуют два соединения: карбон монооксид СО и карбон диоксид СО2.
Очевидно, что с одной и той же массой углерода массы кислорода, необходимые для
образование этих двух оксидов, соотносятся как 1 : 2. При взаимодействии железа с
кислородом возможно образование также двух оксидов: ферум(ІІ) оксид FeO и феррум(III) оксид Fe2О3. В этом случае массы кислорода для образования
этих двух оксидов соотносятся как 2 : 3.
Открытие
закона позволило Дальтону сделать такой вывод: молекулы веществ состоят
с определенного целого числа атомов каждого из элементов.
Одним
из важнейших последствий этого открытия стало установление того факта, что атомы
различных элементов отличаются по массе. Это позволило ввести и установить
атомные массы большого количества элементов, взяв за точку отсчета массу атома
Водорода, которую ученый принял за единицу. И хотя большинство атомных масс, установленных
Дальтоном, не соответствовали действительности, потому что он в своих расчетах не
учитывал валентности элементов, его открытие все же стало одним из
важнейших доказательств атомно-молекулярного учения.
Закон
сохранения массы веществ
Общая
масса веществ, вступающих в химическую реакцию, равна общей массе веществ,
образующиеся в результате реакции.
Этот
закон сформулировал в 1748 году выдающийся русский ученый Михаил Васильевич
Ломоносов и независимо от него в 1789 роде
французский ученый А. Лавуазье. Однако работы Ломоносова в этой области были
опубликованы только в начале XX века, поэтому долгое время первооткрывателем
закона сохранения массы в западноевропейской науке считали Лавуазье, и в некоторых
учебниках закон сохранения массы называют законом Ломоносова - Лавуазье.
Закон
сохранения массы имел очень большое значение для становления атомно-молекулярного
учение, потому что он доказывал то, что во время химических реакций атомы не исчезают и
не появляются из ничего. Число атомов и масса каждого атома не изменяется, поэтому
общая масса веществ так же не меняется.
Закон
сохранения массы является частным случаем общего закона природы - закона
сохранения энергии, который утверждает, что энергия изолированной системы является постоянной. С
этой точки зрения суммарная масса вещества при прохождении химической реакции не может
оставаться неизменной, поскольку в химических реакциях энергия выделяется или
поглощается.
Впрочем,
в химических реакциях изменение массы, вызванная выделением или поглощением энергии,
совсем незначительная. Типичный тепловой эффект химической реакции по порядку величины
равна 100 кДж/моль. На основании уравнения Эйнштейна:
Е
= m
∙
с2
изменение массы в химической реакции будет
равняться
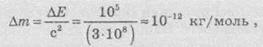
или 10-9 г/моль.
Понятно,
что такое незначительное изменение массы невозможно зарегистрировать экспериментально, а потому
можно утверждать, что в химических реакциях закон сохранения массы выполняется с
высокой точностью.
Закон
объемных соотношений
Закон
объемных соотношений открыл Же. Л. Гей-Люссак в 1808 году, поэтому этот закон также
называют химическим законом Гей-Люссака.
Соотношение
объемов газов, вступающих в химическую реакцию и образуются в результате нее, есть
соотношением простых целых чисел. Так в реакции сжигания метана в кислороде
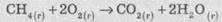
соотношение объемов газов:
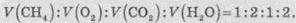
Легко
увидеть, что соотношение объемов газов равно отношению стехиометрических
коэффициентов в уравнении реакции. Конечно же, для выполнения этого закона объемы
газов следует измерять в одинаковых условиях.
Закон Авогадро
Этот
закон открыл выдающийся итальянский ученый Амедео Авогадро в 1811 году.
В
одинаковых объемах различных газов при одинаковых условиях содержится одинаковое
количество молекул.
Это
означает, что все газы ведут себя в определенном смысле одинаково и что объем газа при
заданных условиях не зависит от химической природы газа, а определяется только
количеством частиц. После открытия этого закона свой настоящий смысл и научное
обоснование получил закон объемных соотношений. Большая заслуга Авогадро
заключается в том, что он смог установить простую связь между макроскопической
величине, что наблюдали,- объемом - и микроскопическими свойствами
газообразных веществ - числом частиц.
Анализируя
объемные соотношения Гей-Люссака и используя свое открытие, Авогадро
установил, что молекулы газообразных простых веществ (кислорода, водорода, азота,
хлора) является двохатомними. Если предположить, что водород и хлор одноатомные, то за
счет реакции присоединения объем должен уменьшиться вдвое. Но поскольку объем
не меняется, то молекулы водорода и хлора содержат по два атома, и реакция
проходит по уравнению

Аналогично
можно установить молекулярные формулы воды, аммиака, углекислого газа и других
веществ.
Согласно
с атомно-молекулярным учением, закон Авогадро можно объяснить следующим образом.
Объем, который занимает определенное количество вещества в любом агрегатном состоянии,
обусловлен тремя параметрами: количеством вещества, то есть числом частиц
(молекул, атомов или ионов), расстоянием между молекулами и собственными размерами
частиц. В твердом и жидком агрегатных состояниях вещества расстояние между
частицами очень маленькая, поэтому размеры самих молекул существенно влияют на объем
вещества. Одновременно в газообразном состоянии при обычном давлении расстояние между
молекулами примерно в тысячу раз больше, чем размеры самих молекул, поэтому
размеры молекул можно не учитывать. Вследствие этого объем газов определяется
двумя параметрами: числом молекул и расстоянием между ними. При одинаковых условиях (давление
и температура) расстояние между молекулами в газах одинакова. Отсюда следует, что
объем газа в этом случае определяется только числом молекул. Поэтому в одинаковых
условиях одинаковые объемы различных газов содержат одинаковое число частиц и
наоборот. Следует отметить, что при низких температурах и при высоком давлении
расстояния между молекулами в газах уменьшаются и могут стать соизмеримыми с
размерами молекул, поэтому при таких условиях закон Авогадро не действует.
Выводы
из закона Авогадро.
1. Молярный объем любого газа при нормальных
условий составляет 22,4 л.
(Обоснование
этого вывода см. выше.)
2. Соотношение плотностей двух газов при одинаковых
условий равна соотношению их молярных масс.
Плотность
вещества можно вычислить по формуле:
ρ = m/V.
Если
проводить вычисления для вещества количеством 1 моль, то масса такого количества
будет равняться молярній массе вещества, а ее объем - молярном объема. В этом
случае формула для плотности превратится в следующую:
ρ = m/Vm.
Поскольку,
согласно закону Авогадро, молярные объемы газов при одинаковых условиях равные то
для отношения плотностей двух газов получаем:
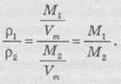
Следовательно,
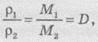
где D - относительная плотность газа - физическое
величина, которая равна отношению плотности какого-либо вещества к плотности другого
вещества, взятой как стандартный образец.
Чистые вещества и смеси
Веществ
в индивидуальном состоянии в природе практически не существует. Они смешаны друг с другом
и образуют смеси и растворы. Смесями являются морская и газированная вода, молоко и
сок, гранит и сталь.
Представление
о смеси и чистые вещества имели еще древнегреческие ученые. В соответствии с этими
представлениями, чистое вещество состоит из частиц одного вида, а смеси
состоят из разных частиц. Итак, чистое вещество состоит из одинаковых молекул,
а смеси - из разных.
Когда
говорят о какой-либо вещество, всегда имеют в виду, что это вещество является чистой
и состоит из частиц одного вида. Но на практике идеально чистое вещество
выделить из смеси невозможно, потому что среди частиц одного вещества
обязательно случится несколько частиц другого вещества, то есть идеально чистых
веществ не бывает. Даже те вещества, которые называют чистыми, содержащие сторонние
частицы других веществ - примеси.
Обычно
абсолютно чистые вещества не нужны, но иногда посторонние примеси могут мешать
проведению опытов. Поэтому, когда речь идет о химические реактивы, обязательно
указывают степень чистоты, такие знаки можно увидеть на банках с химическими
реактивами. Например, если на этикетке написано «техн» (техническая), то в такой
веществе примесей содержится много, несколько
процентов. Для опытов такие вещества обычно не используют, хотя в
строительстве, на заводах такой степени чистоты обычно вполне достаточно.
Степень чистоты «Ч» (чистая) или «ХЧ» (химически чистая) означает, что примесей очень
мало, меньше одного процента. «Чистые» реактивы можно использовать для
производства лекарств, а «химически чистые» - для проведения научных опытов. Иногда
нужны очень чистые вещества. Такие реактивы обозначают знаком «ОСЧ» (особо
чистые). Они содержат, как правило, меньше 10-6 процента примесей. Такие
реактивы нужны для проведения очень точных экспериментов, а также при
производстве микросхем для компьютеров. Очистка веществ - это довольно дорогая
операция, поэтому чем чище вещество, тем она дороже.
Чаще
всего по внешнему виду различить отдельные вещества в смеси не удается.
Например, мы не видим, что воздух - это смесь нескольких газов. По внешнему
видом также нельзя определить, что молоко является смесью различных веществ, а большинство
металлических предметов, которые нас окружают, сделаны из сплавов, а не чистых
металлов. Такие смеси называют однородными. Частицы, которые образуют однородные
смеси, настолько малы, что увидеть их невооруженным глазом невозможно.
Тем
время в неоднородных смесях отдельные вещества можно увидеть невооруженным глазом.
В
смеси все вещества (компоненты) сохраняют свои свойства. Например, если
смешать железный порошок с поваренной солью и поднести к этой смеси магнит, то
железо будет привлечен, а соль - нет. А если к этой же смеси добавить воду,
то соль растворится, а железо не растворится. На этом принципе основывается
изготовление материалов, ведь большинство материалов являются смесями. Например, чистое
золото - это очень мягкий и податливый металл. Такое его свойство создает
неудобства для изготовления большинства ювелирных изделий, поэтому в золото
обязательно добавляют определенное количество серебра. Конечно же, цвет такой смеси
(сплава) немного отличается от цвета чистого золота, однако изделия из него
значительно прочнее и не портятся от небольшого удара.
Как
можно отличить чистое вещество от смеси? Если смесь неоднородна и отдельные ее
компоненты видны невооруженным глазом, например крупинки песка в воде. Но
большинство смесей, которые нас окружают, являются однородными и внешне почти не отличаются
от чистых веществ. Чистое вещество всегда однородна, поэтому даже при значительном
увеличении ее составляющие-кристаллики или крупинки имеют одинаковый вид.
Смеси
можно отличить от чистых веществ с различием физических свойств смеси
от физических свойств отдельных компонентов. Несмотря на то, что каждая
вещество придает смеси своих свойств, смесь никогда не имеет таких же
свойств, как и чистые вещества отдельно. Например, смесь олова и свинца
(сплав) будет плавиться при температуре, ниже температуры плавления
чистого олова или свинца. А чай или раствор сахара в воде будет кипеть при более
высокой температуре, чем чистая вода. В этом случае достаточно измерить температуру
плавления или кипения смеси и сравнить результат с данными из справочника.
Чистые
вещества плавятся и кипят при определенной температуре, а смеси - в небольшом
интервале температур. Если в стакан положить немного снега и опустить в него
термометр, то температура снега не станет выше 0 °С, пока он весь не
растает. Если же нагревать парафин, то он начинает плавиться при одной
температуре, а когда становится совсем жидким, термометр будет показывать более высокую
температуру. Итак, парафин является смесью веществ, которые плавятся при разных
температурах.