ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ПРОДУКТЫ ПЕРЕРАБОТКИ УГЛЕВОДОРОДОВ
Углеводороды - основное сырье для
промышленного получения всех других органических веществ. В то же время углеводороды
химически довольно инертны. Вспомните парафин - вещество, из которого изготовлены свечи
(на самом деле, парафин - это смесь углеводородов ряда метана с числом атомов Углерода
в цепи от 19 до 35).
Насыщенные углеводороды не реагируют ни с
кислотами, ни с щелочами. Они не изменяются на воздухе. Да и в земных недрах в
условиях высоких давлений и повышенных температур природные углеводороды сохранились
без изменений не одну сотню миллионов лет, что свидетельствует об их химическую
инертность.
В то же время при достаточном повышении
температуры, особенно в присутствии катализаторов, углеводороды вступают в
химические реакции, которые связаны как с взаємоперетвореннями собственных молекул, так и
с взаимодействием с другими реагентами.
Мы уже упоминали о крекинг, в
результате которого под действием высокой температуры относительно длинные молекулы распадаются
на части. Энергия связи между различными атомами Углерода в цепи разная:

(числа
над черточками - энергия связи в кДж/моль). Из этой схемы видно, между которыми
атомами происходит разрыв - прежде всего в середине молекулы.
Рассмотрим возможные превращения углеводородов
на примере метана.
На первом этапе термического распада
метана, который становится заметным при температуре выше 500 °С, от молекулы
отщепляется атом Водорода с образованием остатка СН3:

Этот остаток молекулы называется
радикалом. Существенной особенностью радикалов является наличие на одной или нескольких
орбиталях молекулы по одному электрону, изображается как •СН3. Этот
запись соответствует схеме электронного строения:
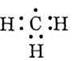
Радикалом, пожалуй, есть и образован под
время разложения метана атом Водорода •Н, но для атомов это понятие, как правило, не
используется, а только для фрагментов, остатков молекул с неспареними
электронами.
Радикалы - весьма реакционно способны
частицы, которые легко вступают в реакции между собой и с другими частицами (как с
молекулами, так и с радикалами). При этом образуются самые разнообразные
соединения.
Как пример, приведем лишь некоторые
продукты, образующиеся из радикалов СН3, СН2 и СН, которые
появились в результате термического разложения метана:

Если в реакционной смеси присутствуют и
другие молекулы, то состав продуктов становится чрезвычайно разнообразным.
Например, при окислении метана
кислородом при повышенных температурах (от 150 до 600 °С) одновременно образуется
много соединений различных классов. В присутствии нескольких катализаторов, которые
ускоряют каждый «свою» реакцию, можно получать различные вещества, среди которых
важнейшие:
метиловый спирт СН3-ОН,
муравьиный альдегид (формальдегид) Н2С=0,
муравьиная кислота 
Одной из важнейших реакций
метана является его конверсия с водяным паром, в результате которой образуется так
называемый синтез-газ:

или смесь водорода с углекислым газом:
