ЧАСТЬ И
ОБЩАЯ ХИМИЯ
НЕКОТОРЫЕ
ПРЕДСТАВИТЕЛИ МЕТАЛЛОВ
Алюминий
Характеристика химического элемента
Алюминий
находится в главной подгруппе III группы, принадлежит к числу редкоземельных металлов.
На внешнем электронном слое содержится три электроны, которые он способен
отдавать.
Сравнивая
Алюминий с другими элементами этой подгруппе, можно отметить неметалічність
Бора, который стоит после Бериллия в периоде металлические свойства Галлия, с чего
можно предположить амфотерности соединений Алюминия, то есть промежуточных (от металлических
в неметаллических) свойств этого элемента.
Распространенность в природе
Алюминий
- самый распространенный металл на Земле (3-е место среди всех элементов; 8% состава
земной коры). В виде простого вещества он в природе не встречается;
входит в состав многих соединений, которые образуют почву; глиноземов (Аl2O3) и бокситов (Аl2O3 ∙
хH2O).
Физические свойства
Алюминий
- серебристо-белый металл. Он ковкий, легко вытягивается в проволоку, tпл = +660 °С, tкип = +2520 °С. При
комнатной температуре алюминий не изменяется на воздухе, потому что его поверхность
покрыта тонкой оксидной пленкой, которая характеризуется сильным защитным действием.
Химические свойства
1) Взаимодействие с кислородом.
Алюминий
является активным металлом, поэтому на воздухе быстро реагирует с кислородом. Но превращению
подвергается только та часть алюминия, которая находится на поверхности образца, поэтому
что продукт взаимодействия - алюминий оксид - образует плотную оксидную пленку:
4Аl + 3О2 = 2Аl2O3.
2) Взаимодействие с галогенами.
Порошкообразный
алюминий активно взаимодействует с йодом при обычных условиях в присутствии каталитической
количества воды:
2Аl + 3И2 = 2АlИ3.
3)
Взаимодействие с серой:
2Аl + 3S = Аl2S3.
4) Взаимодействие с водой.
Несмотря
на высокую химическую активность, с водой алюминий не взаимодействует. В первую очередь, благодаря
защитной пленке, а также потому, что продукт взаимодействия алюминия с водой -
нерастворимое вещество.
5) Взаимодействие с кислотами.
Аналогично
до всех активных металлов алюминий вытесняет водород из растворов кислот:
2Аl + 6НСl = 2АlСl3 + 3Н2;
2Аl + 3Н2SO4 = Аl2 (SO4)с + 3Н2.
6)
Взаимодействие со щелочами.
Благодаря
потому, что алюминий образует амфотерные соединения, он также способен вытеснять водород
из растворов щелочей:
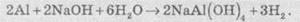
Извлечения алюминия
Алюминий
является одним из многотоннажных продуктов металлургической промышленности. Его добывают
в огромных количествах, потому что он является ценным материалом и реагентом. В
современной металлургии алюминий добывают электролизом бокситов (алюминий оксида).
Поскольку сам алюминий оксид является очень тугоплавкою веществом, для уменьшения
энергозатрат в боксит добавляют плавиковый шпат (кальций фторид), что снижает
температуру плавления руды.
Применение алюминия
Алюминий
является ценным конструкционным материалом. Имея относительную легкость (плотность алюминия
намного легче, чем у стали), он является достаточно прочным металлом. Его используют
для изготовления легких конструкций, в сплаве с магнием для обшивки самолетов
т.д. Из алюминия изготавливают столовые приборы и посуда. В больших количествах
алюминий используют в металлургии для получения металлов алюмотермічним
способом.