ЧАСТЬ И
ОБЩАЯ ХИМИЯ
НЕКОТОРЫЕ
ПРЕДСТАВИТЕЛИ МЕТАЛЛОВ
Кальций
Характеристика химического элемента
Кальций
находится в главной подгруппе II группы, относится к щелочноземельных металлов
вместе с Барием и Стронцием. В наружной оболочке он имеет два электрона и может
легко отдавать их, образуя ионы с устойчивыми конфигурациями инертных газов.
Распространенность в природе
Кальций
имеет большую химическую активность, поэтому встречается в природе только в виде
соединений. Важнейшие природные соединения Кальция: а) известняк, мрамор, мел (СаСО3);
б) гипс (CaSВ4 ∙ 2Н2О); в) фосфорит и апатит
(Са3 (PO4)2); г)
доломит (СаСО3 ∙
MgCO3).
Физические свойства
Кальций
- металл серебристо-белого цвета, очень легкий, как и щелочные металлы, но значительно
тверже и имеет более высокую температуру плавления (+851 °С). Кальций
хранят под слоем керосина.
Добыча
Кальций
добывают путем электролиза его расплавленного хлорида.
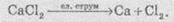
Химические
свойства
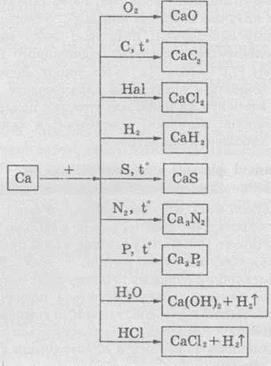
Применение
Важнейшей
соединением Кальция является его карбонат СаС03. Он представляет собой основную составляющую
часть известняка, мрамора, мела, а также входит в состав доломита (MgCО3 ∙ СаСО3). Кальций карбонат используют в
производстве цемента, стали, стекла. Кальций и кальций карбид применяют в
органической химии. А еще Кальций играет очень важную роль в биохимических
процессах, которые протекают в живых организмах.