8. Металлические элементы и их соединения. Металлы
8.3. Металлические элементы главной подгруппы II группы1
8.3.4. Магний гидроксид
Магний гидроксид - нерастворимое в воде вещество белого цвета. При нагревании разлагается:
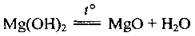
Взаимодействует:
• с кислотными оксидами:
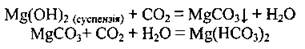
• с кислотами (легко):
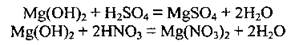
• с амфотерными оксидами (при сплава):
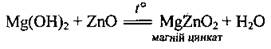
• с амфотерными гидроксидами (сплава):
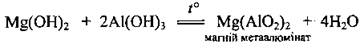
Добыча магний гидроксида
Добывают магний гидроксид действием щелочей или аммиачной водой на растворы солей Магния:
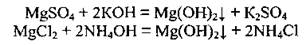
Применение магния и его соединений Магний очень широко используют как основу в производстве легких прочных сплавов для космической и авиационной промышленности, в автомобиле - и приборостроении; в металлургии как восстановитель для извлечения некоторых металлов (например, титана) из их оксидов и галогенидов (магнійтермія):
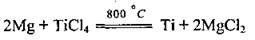
Также его применяют в органическом синтезе.
Яркое пламя горения (в реакции с окислителями) раньше использовали для фотовспышки, а сейчас - в пиротехнике.
Магний оксид через низкую теплопроводность и высокую температуру плавления (выдерживает температуру до 2800 °С) применяют как огнеупорный материал, теплоизолятор (аналогично асбест и тальк), для изготовления некоторых видов цемента, а также огнеупорной керамики.
Магний перхлорат Mg(ClO4)2 используют как водопоглинач для осушки газов (кристаллогидрат содержит шесть молекул воды).
Большие перспективы имеют соединения Магния в электротехнической отрасли (в производстве мощных электрических батарей и сухих элементов).