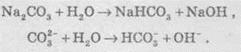ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЯ ЭЛЕМЕНТОВ
КАРБОН.
СИЛИЦИЯ
Карбонаты
Как
уже отмечалось выше, карбонатная кислота образует два типа солей: средние соли
(с анионом СО32-, например, кальций карбонат - СаСО3, натрий карбонат - Na2CO3) и
кислые соли (с анионом НСO3,
например, натрий гідрогенкарбонат - NaHCВ3,
аммоний гідрогенкарбонат - NH4HCВ3).
Карбонаты
и гідрогенкарбонати обычно представляют собой бесцветные или белые кристаллические
соединения (за исключением окрашенного в зеленый цвет минерала малахита -
основного купрум(II) карбоната Сu2(OН)2СO3).
В
воде растворимы только карбонаты щелочных металлов (кроме Лития) и аммония. На
отличие от средних солей, кислые соли, гідрогенкарбонати все растворимые. Растворы
карбонатов и гидрогенкарбонатов проявляют щелочную реакцию за счет реакции
гидролиза:
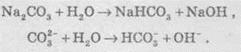
Растворимые
карбонаты металлов (Na2CO3, K2CO3 и (NH4)2CO3) при
нагревании не меняются вплоть до температуры плавления, а нерастворимые карбонаты
при нагревании разлагаются на оксид металла и углекислый газ:
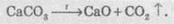
На
отличие от карбонатов, все гідрогенкарбонати растворяются в воде. Однако уже
при несильном нагревании (до +80 °С) гідрогенкарбонати раскладываются согласно
уравнениями:
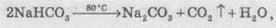
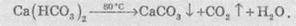
С
этими реакциями люди сталкиваются в быту при кипячении воды в чайнике, ведь
известковый налет на стенках чайника и на нагревательной спирали стиральной машины не
что иное, как смесь карбонатов Кальция, Магния и Железа, образовавшихся при
расписании соответствующих гидрогенкарбонатов.
Все
карбонаты и гідрогенкарбонати взаимодействуют с более сильными кислотами, чем
карбонатная, например с уксусной (СН3СООН) или хлоридной (НСl) кислотами. При этом выделяется
углекислый газ и образуются соответствующие соли:
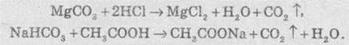
Превращение карбонатов в
гідрогенкарбонати
Поскольку
гідрогенкарбонати представляют собой кислые соли, то они вступают во взаимодействие с
основами. При этом образуются карбонаты и вода:
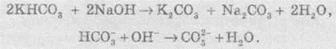
Возможен
также и обратный процесс добывания гидрогенкарбонатов из карбонатов. Для этого
через раствор (или взвесь нерастворимого карбоната) пропускают углекислый газ.
При этом происходят следующие преобразования:
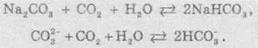
Следовательно,
мы можем объяснить такой эксперимент: через раствор кальций гидроксида (Ca(OH)2) пропускают
углекислый газ. При этом раствор сначала мутнеет, а затем становится снова прозрачным.
Очевидно, что при взаимодействии кальций гидроксида с углекислым газом образуется
нерастворимый кальций карбонат, за что и образуется белая муть:
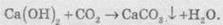
При
дальнейшем пропускании углекислого газа раствор снова становится прозрачным за счет
образование кальций гідрогенкарбонату:
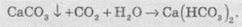
Твердость воды
Твердость
воды - это природное свойство воды, обусловленное присутствием в ней растворенных
солей Кальция и Магния. Суммарную концентрацию ионов Магния и Кальция называют
общей жесткостью воды. Различают постоянную и временную жесткость воды, их
сравнительная характеристика представлена в таблице.
|
Характеристика
|
Временная
твердость, или карбонатная
|
Постоянная
твердость, или некарбонатная
|
|
Причины жесткости
|
Наличие растворенных гидрогенкарбонатов
Магния Mg(HCO3)2 и
Кальция Са(НСО3)2
|
Наличие сульфатов, хлоридов или
некоторых других солей Кальция и Магния (например, CaSВ4, MgCl2 и др.)
|
|
Источники твердой воды
|
Речные и озерные воды, водопроводная
вода, различные газированные минеральные воды
|
Морская вода, вода соленых озер,
природные негазированные минеральные воды
|
|
Устранение жесткости
|
Устраняется при кипячении, при
добавлении кислот или соды (Na2CO3)
|
Не устраняется при кипячении, но
исчезает при добавлении соды (Na2CO3) или при использовании ионообменных смол
|
Морская
вода непригодна для мытья рук через ее твердость - в жесткой воде мыло не
мылится. Твердая вода так же непригодна для стирки, потому что основной
компонент стирального порошка образует химическое соединение с ионами Магния и Кальция.
Естественная умеренная жесткость воды необходима для нормального содержания Кальция в
организме и полноценного развития его костей, но при чрезмерном ее употреблении
появляется вероятность образования в почках камней, которые представляют собой Кальциевые
и Магниевые соли щавелевой кислоты: MgC2В4
- магний оксалат и СаС2О4 - кальций
оксалат;.
В
трубах с горячей водой, в котлах и чайниках откладывается известковый налет,
препятствует нормальному теплообмену и в свою очередь приводит к чрезмерной
расходы топлива, а в дальнейшем и к течи труб, взрыва котлов и плавления чайников.
Для
того чтобы избавиться от известкового налета в чайнике, следует залить его на ночь
столовым уксусом (9% водным раствором уксусной кислоты).
Применение
карбонатов и гидрокарбонатов
|
Название
соединения
|
Формула
соединения
|
Сфера
применение
|
|
Аммоний гідрогенкарбонат
|
NH4HCO3
|
В сельском хозяйстве как
высокоэффективное азотное удобрение и в пищевой промышленности в качестве разрыхлителя теста
|
|
Натрий гідрогенкарбонат (питьевая сода)
|
NaHCO3
|
В медицине и в хлебопекарной
промышленности
|
|
Кальций карбонат
|
СаСO3
|
Наполнитель для бумаги и линолеума,
широко применяется в строительном деле, для добывания извести
|
|
Калий карбонат (поташ)
|
К2СO3
|
Применяют для производства стекла, в
мыловаренной деле, а также как калийное удобрение
|
|
Натрий карбонат (кальцинированная сода)
|
Na2CO3
|
В медицине как знежирювальний средство,
для производства стекла, в качестве наполнителя углекислотных огнетушителей
|
|
Плюмбум карбонат
|
РbСO3
|
Как основной компонент свинцового
белила
|
|
Аммоний карбонат
|
(NH4)2CO3
|
При окраске тканей и при
производстве витаминов
|
|
Барий карбонат
|
ВаСO3
|
При производстве стекла, для
изготовление эмалей и глазури, для борьбы с грызунами
|
Качественная
реакция на карбонат-ион
Для
обнаружение карбонат-иона используют, в основном, две реакции. Первая заключается
в том, что на исследуемый раствор действуют разбавленными минеральными кислотами,
например, сульфатной или хлоридной. При этом, в случае присутствия карбонатов,
выделяются пузырьки углекислого газа, образующегося за такой реакцией:
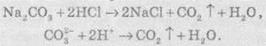
В
качественном анализе также используют тот факт, что карбонаты щелочноземельных
металлов нерастворимы в воде. Тогда к исследуемому раствору добавляют соль Кальция
или Бария, в результате чего в растворе образуется белая муть: