8. Металлические элементы и их соединения. Металлы
8.1. Общие сведения о металлические элементы и металлы
8.1.5. Общие способы получения металлов
В виде самородных металлов случается незначительное количество малоактивных металлов: золото, платина, серебро. Большинство металлических элементов встречается в природе в виде соединений - оксидов, сульфидов, сульфатов, хлоридов, карбонатов, нитратов, ортофосфатов - руд.
Руда - природное минеральное сырье, содержащее металлы и их соединения в количествах и виде, пригодных для их промышленного использования (металлическая руда). Различают:
• полиметаллические руды, содержащие свинец, цинк и обычно медь и как постоянные примеси - серебро, золото, иногда кадмий, индий, галлий и некоторые другие редкие металлы;
• радиоактивные руды содержат металлы радиоактивных элементов (уран, радий, торий);
• комплексные руды - сложная по содержанию сырье, из которого экономически выгодно добывать несколько металлов или других полезных компонентов. Например, медно-никелевая руда, из которой, кроме никеля и меди, добывают кобальт, металлы платиновой группы, золото, серебро, селен, теллур, серу.
Иногда рудой называют также некоторые виды неметаллического минерального сырья: асбестовая, баритова, графитовая, фосфорная, серная, агрономическая руда1.
3а содержанием полезного компонента руды разделяют на:
• природно-богатые - содержание полезного компонента в 2-3 раза выше кондиционных (пригодного для непосредственного использования);
• средние - содержание полезного компонента равна или на 10-50 % выше кондиционного;
• бедные (требуют обогащения) - содержание полезного компонента на грани кондиционного.
С течением времени и развитием добывающей и перерабатывающей промышленности растут и возможности использования бедных источников сырья. В условиях исчерпания ресурсов природно-богатых месторождений бедные руды могут переходить в разряд средних.
Решением проблемы извлечения металлов из природных соединений занимается наука и промышленная отрасль - металлургия. Различают черную (металлургию железа) и цветную металлургию (металлургию всех других металлов). Последнюю условно разделяют на металлургию тяжелых (медь, свинец, цинк, олово, никель) и легкие (алюминий, титан, магний) металлов. Химизм металлургических процессов заключается в восстановлении металлических элементов:
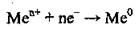
Восстановление осуществляют с помощью различных восстановителей, благодаря чему получают металлы в чистом виде. Восстанавливают металлы с помощью кокса (углерода), карбон(II) оксида, водорода, активных металлов (алюминия, магния), а также постоянного электрического тока.
Значительная часть металлургических процессов основывается на восстановлении оксидов металлических элементов. Если же используют сульфидные руды, то их предварительно нагревают за наличия воздуха (выжигают). При этом сульфид металлического элемента превращается в оксид:
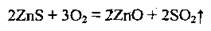
В зависимости от природы восстановителя и условий протекания реакции восстановления, различают:
• пірометалургію;
• гідроелектрометалургію;
• электрометаллургии.
Пірометалургія - это отрасль металлургии, где проводят восстановление металлов из руд за очень высокой температуры с помощью различных восстановителей (С, CO, Н2, Al, Mg):
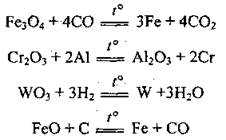
При осуществлении реакций с участием активных металлов или кокса получают расплавы металлов, а при использовании газообразных восстановителей (Н2, СО) добывают металлические порошки (порошковая металлургия). Другой разновидностью пірометалургії есть плазменная металлургия, которая дает возможность восстанавливать металлы непосредственно из руд. Ее недостатком является высокая энергоемкость.
Гидроэлектрометаллургия. Этот путь получения металлов с помощью водных растворов предусматривает осуществление двух процессов:
1) перевод естественного соединения определенного металлического элемента (оксида, соли) в раствор путем растворения в кислоте:
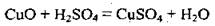
2) восстановление металла из полученного раствора соли:
• с помощью более активного металла:
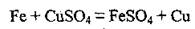
• электролизом.
В общем электролиз растворов используют для извлечения из руд значительного количества металлов, прежде всего цветных и благородных: Cu, Ві, Sb, Sn, Pb, Ni, Co, Cd, Zn, Mn, Cr. Сегодня около 20 % мирового производства меди, 50-70 % цинка и никеля, 100 % алюминия и урана (из их оксидов), кадмия, кобальта и др базируется на гидроэлектрометаллургии (электроэкстракции).
Электрометаллургия - это добыча металлов электролизом расплавов солей. Так добывают, например, щелочные, щелочноземельные металлы. Собственно, это единственный способ их добывания, поэтому в особенности оксиды этих металлических элементов невозможно восстановить коксом, водородом или карбон(II) оксидом.
_____________________________________________________________
1 Используют для производства минеральных удобрений или для улучшения почвы в агрономических целях.