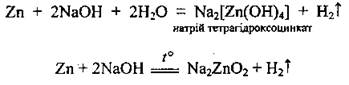8. Металлические элементы и их соединения. Металлы
8.1. Общие сведения о металлические элементы и металлы
8.1.3. Общие химические свойства металлов
Самый типичный признак металлических элементов - это способность относительно легко отдавать электроны:
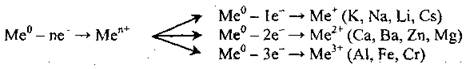
1. Взаимодействие металлов с простыми веществами (неметаллами):
а) с галогенами. Образуются соответствующие соли - галогениды:
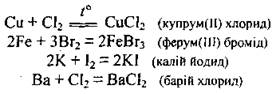
б) с кислородом. Обычно образуются оксиды, с некоторыми металлами - пероксиды, надпероксиди:
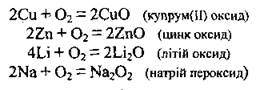
в) с азотом:
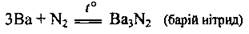
г) с фосфором:
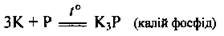
г) с серой:
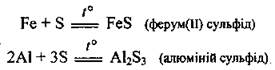
д) с водородом. Самые активные металлы соединяются с водородом, образуя гидриды:
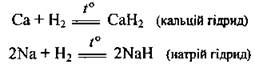
е) с углеродом. Образуются карбиды:
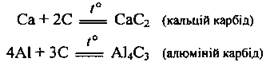
2. Реакции металлов с водой. Химическая активность металлов в реакциях с водой определяется их размещением в ряду активности металлов. При обычных условиях с водой реагируют только самые активные металлы (щелочные и щелочноземельные). Образуются соответствующие щелочи и водород:
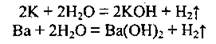
Заметим, что в аналогичные реакции могут вступать магний (при нагревании) и алюминий (после снятия оксидной пленки). За очень высокой температуры с водой (водяным паром) взаимодействуют некоторые менее активные металлы (цинк, железо). Во время таких реакций образуются не гидроксиды, а оксиды:
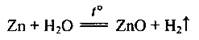
3. Реакции металлов с кислотами. Химическая активность металлов в реакциях с растворами кислот также определяется размещением металла в витискувальному ряду. Металлы, расположенные левее водорода, взаимодействуют с такими кислотами, как хлоридная НСl, фосфатная Н3РO4, сульфатная H2SO4 (разбавленная). Образуется соль и выделяется водород.
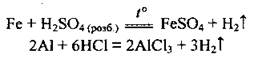
Те же металлы, которые размещаются после водорода, с приведенными кислотами не реагируют.
Заметим, что разбавленная азотная и концентрированная сульфатная кислоты являются сильными окислителями, поэтому они реагируют с металлами, которые в ряду активности металлов размещены слева и справа от водорода, но водород в этих реакциях не выделяется:
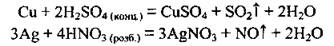
4. Взаимодействие металлов с солями. Для установления возможности реакции между металлом и солью (раствор) используют ряд активности металлов. Реакция происходит, если металл-реагент является более активным (т.е. в ряду активности размещается левее), чем металл, который образуется (продукт реакции):
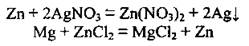
5. Взаимодействие металлов со щелочами. Со щелочами взаимодействуют только те металлы, которым соответствуют амфотерные оксиды и гидроксиды (алюминий Аl, цинк Zn, олово Sn...). Такие реакции могут происходить с использованием не только водного раствора и расплава щелочи: