ОТ НАТРИЯ ДО АРГОНА
СВОЙСТВА ОКСИДОВ И ГИДРОКСИДОВ
В оксидах и гідроксидах, образованных
элементами 3-ого периода, можно наблюдать оба типа химической связи - ионный
и ковалентная. Напомним, что гидроксиды можно рассматривать как продукты взаимодействия
оксидов с водой. В данном случае гидроксидами являются как основа
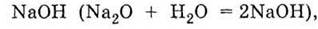
так
и кислота Н2SO4 (SО3 + Н2O = Н2SO4). Оксиды (и гидроксиды-основания)
металлов - ионные, а оксиды (и гидроксиды-кислоты) неметаллов (и металлов высокой
валентности, например СrO3 илиn2O7) - ковалентные соединения.
Соответственно различают и их
свойства - основные и кислотные. При этом существует как плавный переход от ионного
связи к ковалентной, так идентично имеет место непрерывный переход от
соединений основного характера (основ, основных оксидов) до соединений кислотного
характера (кислот, кислотных оксидов).
Принадлежность гидроксида основ
или кислот определяется с помощью индикатора и его реакций с другими
гидроксидами (кислотами или основаниями). Индикатор не меняет окраску в
практически нерастворимых веществах, например, в гидроксиде алюминия и силикатному
кислоте.
Согласно свойств
гидроксидов классифицируются по свойствам и оксиды элементов 3-го периода:
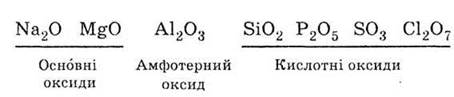
Амфотерные свойства оксида
алюминия проявляются в его способности взаимодействовать с кислотными оксидами (и
кислотами), например:
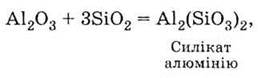
и
с основными оксидами и основаниями, например:
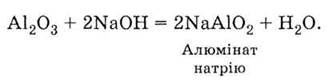
Важным свойством оксидов является их
способность взаимодействовать с водой. Существует общее правило: с водой взаимодействуют те
оксиды, которые образуют растворимые в воде соединения.
Рассмотренные в этом параграфе
закономерности характерны для оксидов и гидроксидов элементов всех периодах
периодической системы элементов.