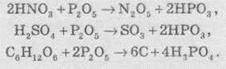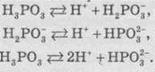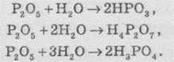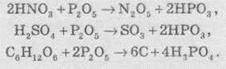ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЯ ЭЛЕМЕНТОВ
НИТРОГЕН. ФОСФОР
Оксиды фосфора
Фосфор
образует два оксиды - Р2O3 , P2O5. Это упрощенные
формулы веществ. На самом деле молекулы оксидов Фосфора имеют такой состав: Р4O6 и Г4O10.
Физические
свойства оксидов Фосфора
Фосфор(III)
оксид Р2O3
(фосфітний ангидрид) представляет собой легкоплавкую вещество (Тпл = +24 °С,
Ткип = +175 °С). Он растворяется в некоторых органических растворителях и
в сірковуглецеві, а также в фосфатной и фосфітній кислоте, и имеет резкий запах.
Фосфор(V) оксид Р2O5 (фосфатный ангидрид) в обычных условиях является
белой, очень гигроскопичным веществом. Плотность твердого фосфатного ангидрида
равна 2,3 г/см3. При его нагревании до +359 °С происходит фазовый
переход из твердого состояния в газообразное, минуя жидкое. Такой фазовый
переход называют сублимацией.
Химические
свойства
оксидов Фосфора
Оба
оксиды Фосфора являются кислотными оксидами.
Химические свойства фосфітного
ангидрида
Р2O3 активно реагирует
с водой. При этом образуется двохосновна фосфітна кислота Н3РO3 средней силы:
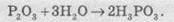
В
твердом состоянии это бесцветное гигроскопичное кристаллическое соединение с температурой
плавления +74 °С. В водных растворах происходит диссоциация по схеме (Ка1 = 2 ∙ 10 3, Ка2 = =6 ∙ 10-7):
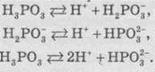
При
реакции Р2O3
со щелочами образуются соли фосфітної кислоты - фосфіти:
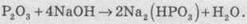
Фосфор
триоксид, фосфітна кислота и ее соли проявляют четко выраженные восстановительные свойства.
Например, фосфітна кислота восстанавливает малоактивные металлы из их водных
растворов:
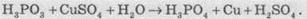
Кислород
воздух - триоксид окисляет фосфор в пентаоксид:
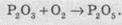
Химические свойства фосфатного
ангидрида
Фосфор(V) оксид очень активно взаимодействует с водой.
При этом может образовываться три кислоты: метафосфатна (НРO3), пірофосфатна
(Н4Р2O7)
или ортофосфатная (Н3РO4). Продукты
реакции зависят от количества воды:
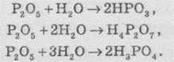
Для
того чтобы увидеть сходство этих кислот, их можно рассматривать как гидраты фосфор
оксида:
|
НРO3
|
0,5 (Р2O5 ∙ Н2O)
|
|
H4P2O7
|
1 (Р2O5 ∙ 2Н20)
|
|
Н3РO4
|
0,5 (Р2O5 ∙ 3Н2O)
|
Для
упрощение вместо формул фосфатных кислот в большинстве уравнений реакции записывают
формулу ортофосфатной кислоты Н3РO4.
Р2O5 проявляет
свойства кислотного оксида. Он реагирует с щелочами и основными оксидами, при
этом образуются соли фосфорной кислоты - фосфаты:
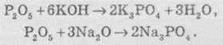
Фосфор
пентаоксид очень активно поглощает влагу из воздуха. Давление паров воды над поверхностью
Р2O5
составляет всего 0,00002
мм рт. ст. (для сравнения: давление паров над поверхностью
концентрированной серной кислоты равна 0,003 мм рт. ст., т.е.
примерно в 100 раз больше).
Фосфатный
ангидрид отщепляет молекулы воды от многих соединений. Например, при действии Р2O5 на кислоты
образуются соответствующие ангидриды кислот, а много органических соединений при действии фосфор
оксида обугливаются: