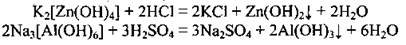РАЗДЕЛ II. НЕОРГАНИЧЕСКАЯ ХИМИЯ
7. Основные классы неорганических соединений
7.5. Амфотерные соединения
7.5.2. Амфотерные гидроксиды
Амфотерные гидроксиды - это гидраты амфотерных оксидов, которым присущи слабые основные свойства, а также слабые кислотные свойства. Все амфотерные гидроксиды - это белые твердые вещества, которые не растворяются в воде:
• Zn(OH)2 - цинк гидроксид
• Сr(ОН)3 - хром(III) гидроксид
• Аl(ОН)3 - алюминий гидроксид
• Рb(ОН)2 - свинец(II) гидроксид
• Fe(OH)3 - феррум(III) гидроксид
• Ве(ОН)2 - бериллий гидроксид
Химические свойства
1. Амфотерные основания - очень слабые электролиты. Поскольку полярности связей Ме-О и Н-О близки, амфотерные гидроксиды могут диссоциировать с образованием незначительных количеств ионов Водорода и гидроксил-ионов:
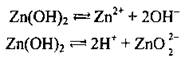
В растворах амфотерных гидроксидов индикаторы не изменяют своей окраски.
2. Амфотерные основания растворяются в кислотах:
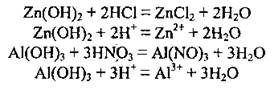
3. Амфотерные основания взаимодействуют с щелочами:
а) твердые щелочи взаимодействуют с амфотерными основаниями при сплава:
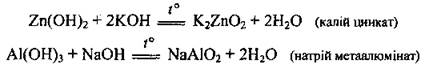
Однако возможно образование и солей - ортоалюмінатів:
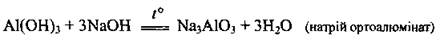
б) в растворах щелочей образуются комплексные соли:
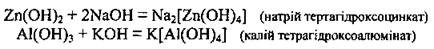
или при избытке щелочи:
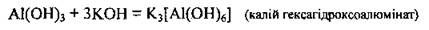
Добыча амфотерных гидроксидов
Для их получения используют 2 способа:
1) взаимодействие соответствующих солей со щелочами:
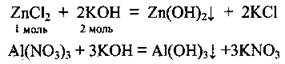
2) взаимодействие комплексных солей с растворами кислот: