2-й семестр
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
1. Свойства газов, жидкостей, твердых тел
Урок 7/78
Тема. Основное уравнение МКТ идеального газа
Цель урока: выяснить механизм давления идеального газа и его зависимость от микропараметров
Тип урока: изучение нового материала
План урока
Контроль знаний |
5 мин. |
1. Закон Гей-Люссака.
2. Закон Шарля.
3. Закон Бойля-Мариотта.
4. Графики изопроцесса |
Демонстрации |
3 мин. |
1. Модель давления газа.
2. Фрагмент кинофильма «Молекулы и молекулярное движение» |
Изучение нового материала |
25 мин. |
1. Основное уравнение молекулярно-кинетической теории идеального газа.
2. Связь давления со средней кинетической энергией молекул |
Закрепление изученного материала |
12 мин. |
1. Тренируемся решать задачи.
2. Контрольные вопросы |
ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА
1. Основное уравнение молекулярно-кинетической теории идеального газа
Основная задача молекулярно-кинетической теории газа заключается в том, чтобы установить соотношение между давлением газа и его микроскопическими параметрами - массой молекул, их средней скоростью и концентрацией. Это соотношение называется основным уравнением молекулярно-кинетической теории газа.
Поскольку давление газа на стенку сосуда обусловлено ударами молекул, давление газа пропорционально концентрации молекул n: чем больше молекул в единице объема, тем больше ударов молекул о стенку за единицу времени. Каждая молекула при ударе о стенку передает ей импульс, пропорциональный импульсу молекулы, равном по модулю m0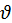 , где
, где 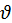 - модуль скорости молекулы. Поэтому можно было бы ожидать, что давление пропорционально nm0
- модуль скорости молекулы. Поэтому можно было бы ожидать, что давление пропорционально nm0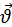 , где
, где 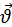 - среднее значение модуля скорости молекул.
- среднее значение модуля скорости молекул.
Однако, на самом деле давление пропорционально не первой, а второй степени скорости, так как, чем больше скорость молекулы, тем чаще она бьется о стенку сосуда. И действительно, расчеты показывают, что основное уравнение молекулярно-кинетической теории идеального газа имеет вид:
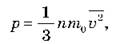
где m0 - масса одной молекулы газа, n - концентрация молекул, 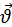 2 - среднее значение квадрата скорости молекул.
2 - среднее значение квадрата скорости молекул.
Коэффициент 1/3 обусловлен трехмерностью пространства - тем, что во время хаотического движения молекул все три направления равноправны.
Итак, немецкий физик Г. Клаузиус выяснил, что давление идеального газа прямо пропорционально концентрации частиц, массы частицы и среднего значения квадрата скорости частицы.
Полученное уравнение связывает макроскопічну величину - давление,- что может быть измерено манометром, с микроскопическими величинами, характеризующими молекулы, и является как бы мостиком между двумя мирами: макроскопическим и микроскопическим.
2. Связь давления со средней кинетической энергией молекулы
Если через 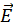 обозначить среднюю кинетическую энергию поступательного движения молекулы,
обозначить среднюю кинетическую энергию поступательного движения молекулы, 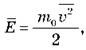 то уравнение Клапейрона можно записать в виде:
то уравнение Клапейрона можно записать в виде:
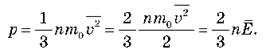
Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы В этой формуле концентрация частиц характеризует число ударов молекул о поршень, а средняя кинетическая энергия молекул определяет интенсивность одного удара.
Вопрос к ученикам во время изложения нового материала
1. Каков механизм возникновения давления газа с точки зрения молекулярно-кинетической теории строения вещества?
2. Почему можно считать, что молекулы в газе движутся только вдоль трех взаимно перпендикулярных направлений?
3. В каких слоях атмосферы воздух по своим свойствам приближается к идеальному газу: у поверхности Земли или на далеких высотах?
ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО МАТЕРИАЛА
1). Тренируемся решать задачи
Кислород находится в нормальных условиях. Вычислите среднюю квадратичную скорость молекул газа.
Решение
При нормальных условиях давление кислорода равна 1,01·105 Па, а плотность - 1,43 кг/м3. Считая, что концентрация газа n = N/V, можно записать:
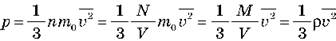
Отсюда получаем: 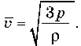
Проверив единицы величин и выполнив расчеты, получаем 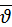 = 460 м/с.
= 460 м/с.
2. Определите кинетическую энергию хаотического поступательного движения всех молекул любого газа в баллоне объемом 5 л с давлением 1 МПа.
3. Чему равна средняя кинетическая энергия хаотического движения молекул аргона, если 2 кг его, находясь в сосуде объемом 2 м3, оказывают давление 3·105 Па?
2). Контрольные вопросы
1. Каким образом в основном уравнении молекулярно-кинетической теории мы получили множитель 1/3?
2. Почему молекула при столкновении со стенкой сосуда действует на нее с силой, пропорциональной скорости, а давление пропорционально квадрату скорости?
3. Как средняя кинетическая энергия молекул зависит от концентрации газа и его давления на стенки сосуда?
Что мы узнали на уроке:
• Давление идеального газа прямо пропорционально концентрации частиц, массе частицы и среднему значению квадрата скорости частицы.
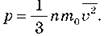
• Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы:
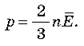
Домашнее задание
1. Конспект.
2. Решите задачи:
г1): 1. Как изменится давление газа, если концентрация его молекул увеличится в 3 раза, а средняя квадратичная скорость молекул уменьшится в 3 раза?
2. Под каким давлением находится газ в сосуде, если средняя квадратичная скорость его молекул 103 м/с, концентрация молекул 3·1025 м-3, а масса каждой молекулы 5·10-26 кг?
3. Определите среднюю кинетическую энергию поступательного движения молекул газа с давлением 105 Па. Концентрация молекул газа 2,7·1025 м-3.
р2): 1. Определите плотность кислорода, находящегося под давлением 1,3·105 Па. Средняя квадратичная скорость молекул 1,4·103 м/с.
2. Какое давление на стенки сосуда оказывают молекулы газа, если масса газа 3 г, объем 5·10-4 м3, средняя квадратичная скорость молекул 500 м/с?
3. Какова средняя квадратичная скорость движения молекул газа, который занимает объем 5 м3 с давлением 2·105 Па и имеет массу 6 кг?
Г3): 1. Давление углекислого газа, если в баллоне объемом 40 л содержится 5·1024 молекул, а средняя квадратичная скорость молекул 400 м/с?
2. Определите кинетическую энергию хаотического поступательного движения всех молекул любого газа в баллоне объемом 10 л и давлением 4·105 Па.
3. Часть стенки сосуда покрыли клеем, что поглощает все падающие молекулы газа. Изменится ли давление газа на этот участок стенки? Обоснуйте свой ответ.