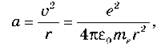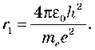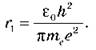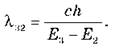|
УРОК 1/78 Тема урока: Постулаты Бора
Цель урока: ознакомить учащихся с ядерной моделью атома; раскрыть пути выхода из кризиса классической физики. Тип урока: урок изучения нового материала. ПЛАН УРОКА
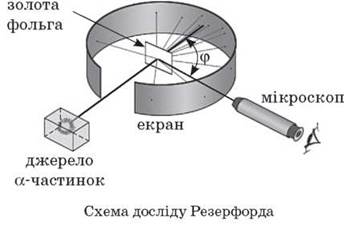
ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА Эксперименты, проведенные различными учеными на протяжении XIX столетия, доказали, что атом имеет сложную структуру. Физикам стало известно, что в состав атома входят электроны, которые имеют отрицательный заряд, хотя атом в целом является нейтральным. Одну из первых моделей атома 1903 г. предложил Томсон. Согласно модели Томсона атомы представляют собой однородные шарики из положительно заряженного вещества, в которой находятся электроны. Суммарный заряд электронов равен положительному заряду атома. Поэтому атом в целом электрически нейтрален. Эта модель получила название «пудинг», потому что электроны были вкраплены в положительно заряженное среду, подобно изюму в пудинге. Дальнейший прогресс в исследовании внутренней структуры атома был связан с именем английского физика Эрнеста Резерфорда. Резерфорд предложил своим сотрудникам экспериментально проверить способность модели атома Томсона. Пропуская через очень тонкую металлическую пленку узкий пучок быстрых
Потерпев рассеяния в золотой фольге, Резерфорду понадобилось несколько лет, чтобы окончательно понять столь неожиданное рассеяния Резерфорд смог определить размер атомного ядра. И оказалось, что атомное ядро в десятки тысяч раз меньше собственно атома: размер ядра - порядка 10-14-10-15 м, в то время как размер атома примерно 10-10 м. Основываясь на своих опытах и расчетах, Резерфорд предложил планетарную (ядерную) модель атома: • атомы любого элемента состоят из положительно заряженной части, получившей название ядра; • в состав ядра входят положительно заряженные элементарные частицы - протоны (позже было установлено, что и нейтральные нейтроны); • вокруг ядра вращаются электроны, образующие так называемую электронную оболочку. Подобие атома с Солнечной системой усугублялась тем, что закон Кулона, что «управляет» движением электронов, совпадает по форме с законом всемирного тяготения, что «управляет» движением планет: и в том, и в другом случае сила обратно пропорциональна квадрату расстояния. Согласно классической теории, система, состоящая из массивного положительно заряженного ядра и легких, отрицательно заряженных электронов, может быть устойчивой только в том случае, когда электроны находятся в движении. Таким образом, атом должен быть подобен миниатюрной Солнечной системе, в которой роль Солнца играет ядро, а планет - электрон. Двигаясь по «планетарных» орбитам, электроны должны были бы путем излучения терять энергию движения и в результате быстро приближаться к ядру. Расчеты показывали, что электрон в атоме Водорода должен випроменити всю свою энергию за малую долю секунды. Однако в атоме этого не происходит. Таким образом, в «атомных масштабах» противоречит опыту не только классическая электродинамика, но и классическая механика - основа основ всей классической физики. Датский физик Нильс Бор дополнил планетарную модель атома положениями, которые призваны были устранить недостатки этой модели. в 1913 году опубликовал свою квантовую теорию атома. Основу этой теории составляют постулаты Бора. Первый постулат Бора: Ø Существуют особые состояния атома, в которых он не излучает энергию. Такие состояния называют стационарными состояниями. Ø Стационарное состояние атома означает, что его электроны локализованы в пространстве и имеют определенную энергию. Момент импульса тела определяют как L = m
где me - масса электрона; В ядерной физике часто используют величину Второй постулат Бора: Ø Любое излучение атома связано с его переходом из одного стационарного энергетического состояния в другое. Ø Для перехода атома из одного стационарного состояния в другое со значениями энергий E1 и E2 выполняется равенство:
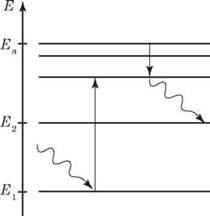
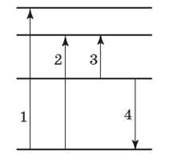
Для наглядной демонстрации энергетического состояния атома применяют специальные схемы. Каждый стационарный (разрешенный) состояние атома обозначают линией, которую называют энергетическим уровнем. Самый низкий уровень называют энергетическим уровнем основного состояния. Выше него расположены другие разрешенные уровне. Переходы атома из одного состояния в другое изображают вертикальными стрелками.
На рисунке показаны энергетические уровни атома Водорода. По теории Бора следует формула для энергии любого возбужденного состояния атома Водорода: Все энергетические уровни соответствуют отрицательным значениям энергии: нулевое значение энергии соответствовало бы удалению электрона на бесконечно большое расстояние от ядра, то есть ионизации атома. Самый низкий энергетический уровень соответствует основному состоянию атома, а все остальные - возбужденным. Для ионизации атома, находящегося в основном состоянии, необходимо передать ему энергию, равную |E1| (это так называемая энергия ионизации атома). Теория Бора дает правильное значение энергии ионизации атома Водорода: 13,55 эв. Теперь можно объяснить, почему атомы являются стабильными: без поступления энергии извне они могут переходить только в состояние с меньшей энергией. Обычно атом находится в возбужденном состоянии недолго (около 10-8 c), после чего переходит в основное состояние. Если же атом находится в основном состоянии, то переходить ему некуда. Существование основного состояния (состояния с наименьшей энергией) является общим признаком квантовых систем. Наибольший успех теория Бора имела применительно атома Водорода, для которого оказалось возможным построить количественную теорию. Однако уже для следующего по сложности атома - Гелия - добиться количественного согласия с опытом не удалось, не говоря уже о более сложные атомы. Дальнейшее развитие физики показало, что трудности теории Бора были связаны с ее внутренней противоречивостью, потому что в ней сочетались законы классической физики и противоречащие им постулаты Бора. ВОПРОС К УЧАЩИМСЯ В ХОДЕ ИЗЛОЖЕНИЯ НОВОГО МАТЕРИАЛА Первый уровень 1. В чем заключаются различия между моделями атома, предложенной Томсоном и Резерфордом? 2. Каким экспериментальным данным противоречит планетарная модель атома? 3. От чего зависит частота излучаемого атомом света? 4. В каком состоянии энергия электрона меньше: в основном или в возбужденном? Второй уровень 1. Почему планетарная модель атома не согласуется с законами классической физики? 2. Почему планетарная модель атома не могла объяснить сходство атомов? 3. Какими способами можно перевести атом в возбужденное состояние? ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО МАТЕРИАЛА 1. Можно ли применять закон Кулона для вычисления силы взаимодействия альфа-частицы с ядром атома золота в опыте Резерфорда? 2. Которые классические представления о движении и взаимодействии частиц положены в основу теории Бора? 3. В результате изменений, происходящих в атоме, возникает излучение? 1. Определите радиус первой орбиты атома Водорода. Решения. Центростремительному ускорению электрона определено кулоновским силой притяжения к ядру атома Водорода:
где ε0 - электрическая постоянная. Орбитальный момент импульса электрона на первой орбите: me
Запишем уравнение для r1: Учитывая то, что ђ = h/2 Проверив единицы величин и подставив численные значения, получаем, что радиус первой орбиты атома Водорода равна 5,31 · 10-11 м. 2. На рисунке показаны энергетические уровни атома. Стрелками обозначены переходы между уровнями. При каких переходов происходит поглощение излучения? За которого перехода выпускается излучения максимальной длины волны? За которого перехода выпускается излучения максимальной частоты?
3. На сколько изменилась энергия электрона в атоме Водорода при излучении атомом фотона с длиной волны 4,86 · 10-7 м? 4. Воспользовавшись рисунком, на котором показаны энергетические уровни атома Водорода, определите длину волны излучения, соответствующий переходу между первыми и вторым возбужденными состояниями атома водовода. Решения. Первый возбужденное состояние соответствует второму снизу энергетическому уровню (n = 2), а второй возбужденное состояние - третьем (n = 3). Энергия фотона, что соответствует переходу между этими энергетическими уровнями, hv32 = E3 - E2. Поскольку длина волны λ32 = c/v32, получаем Проверив единицы величин и подставив числовые значения в СИ (E2 = -5,4 · 10-19 Дж, E3 = -2,4 · 10-19 Дж), получаем: λ32 = 6,6 · 10-7 м. 5. При переходе атома Водорода из четвертого энергетического состояния во второе излучаются фотоны с энергией 2,55 эв. Определите частоту излучения. ЧТО МЫ УЗНАЛИ НА УРОКЕ • Постулаты Бора. 1. Существуют особые состояния атома, в которых он не излучает энергию. Такие состояния называют стационарными состояниями. 2. Любое излучение атома связано с его переходом из одного стационарного энергетического состояния в другое: hv = E1 - E2. • Формула для энергии любого возбужденного состояния атома Водорода: Домашнее задание 1. Подр-1: § 50; подр-2: § 25 (п. 1, 2). 2. Сб.: Рів1 № 16.1; 16.2; 16.3; 16.4. Рів2 № 16.9; 16.10; 16.11; 16.12. Рів3 № 16.16, 16.17; 16.18; 16.19.
|
|