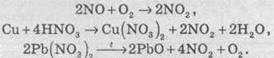|
Нитроген(II)
оксид Нитроген(II)
оксид представляет собой бесцветный газ с низкими температурами плавления и кипения
(Тпл = -164 °С, Ткип = -152 °С). Он плохо растворяется
в воде. С щелочами и кислотами-неокисниками нитроген(II) оксид не взаимодействует. Для
промышленного использования его добывают каталитическим окисненням аммиака:
В
лабораторных масштабах нитроген(II) оксид добывают действием 30 % азотной кислоты
на металлическую медь:
При
разряде молнии он образуется из азота и кислорода атмосферы. Этот газ является одним
из главных источников соединений азота в почве Земли:
На
воздухе быстро окисляется, при этом образуется бурый газ:
Нитроген(II)
оксид проявляет окислительные свойства:
Его
применяют для производства серной и азотной кислот. Нитроген(ИV) оксид Нитроген
диоксид представляет собой газ (Тпл = -11 °С, Ткип = +21 °С)
характерного бурого цвета с неприятным, «жгучим» запахом. NВ2 обычно добывают азот окисненням
монооксида кислородом воздуха, или взаимодействием меди с концентрированной нітратною
кислотой, или термическим разложением нитратов малоактивных металлов:
Газ
реагирует с водой, при этом происходит реакция диспропорціонування:
В
результате этой реакции образуется сильная азотная кислота HNВ3 и слабая неустойчивая нітритна кислота HNВ2. При взаимодействии бурого газа с раствором
щелочи образуются две соли - нитрат (соль азотной кислоты) и нитрит (соль
нітритної кислоты):
Нитроген
диоксид при низких температурах заметно димеризований (то есть две одинаковых молекулы
соединяются в одну):
N2В4 - это бесцветная жидкость, при нагревании
разлагается на две молекулы нитроген(II) оксида. Нитроген
диоксид используют при производстве азотной кислоты как хороший нітрувальний
агент (вещество, что позволяет добавить в состав NO2).
|
|