ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЯ ЭЛЕМЕНТОВ
НИТРОГЕН. ФОСФОР
Химические
свойства простых веществ
Химические
свойства азота
Азот
представляет собой очень устойчивую инертную соединение. Атомы Азота связаны в молекулу
тройной связью: одним σ-связью
и двумя π-связями.
Для разрушения такой молекулы на атомы необходимо затратить огромное количество
энергии. Например, при 3000 °С диссоциация молекулы на атомы происходит не
более чем на 0,5%. За счет высокой устойчивости молекулы простое вещество ведет себя
достаточно пассивно. При обычных условиях азот вступает в реакцию только с металлическим
литием:
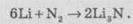
При
нагревании азот взаимодействует с некоторыми металлами и неметаллами, при этом
образуются нитриды, соединения, в которых Азот проявляет степень окисления -3:
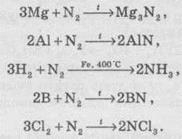
В
электрическом разряде азот реагирует с кислородом, при этом образуются оксиды
Азота II и IV. За счет этого во время грозы воздух, а впоследствии и почву,
обогащается сложными соединениями Азота:

Реакции
со сложными соединениями для азота не характерны, однако в XIX веке при
производстве аммиака воспользовались такой реакцией с кальций при карбидом
нагревании:
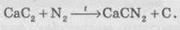
Химические
свойства фосфора
Химические
свойства всех алотропних модификаций фосфора одинаковые, за исключением того, что
белый фосфор активнее, чем красный, а красный активнее, чем черный. Таким
образом, вещество фосфор при составлении химических реакций будем записывать просто
как Г. Красный и черный фосфор реагируют с кислородом воздуха при повышенной
температуре, а белый - даже при комнатной температуре:

Белый
фосфор при медленном окислении кислородом воздуха излучает свет. Это
происходит вследствие того, что в процессе окисления энергия, которая выделяется,
расходуется на излучение света. Это явление называют хемілюмінесценцією.
Фосфор
реагирует с некоторыми неметаллами-окислителями, при этом могут образовываться производные
Фосфора с разной степенью окисления. Это зависит от количества
вещества-окисника. При избытке окисника образуются соединения Фосфора(V), а при недостатке Фосфора(III):
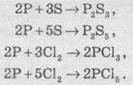
Фосфор
вступает во взаимодействие со многими активными металлами. При этом образуются
фосфиды металлов. Фосфиды - это соединения, в которых атом Фосфора проявляет степень
окисления -3:
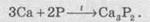
С
водородом прямая реакция не проходит, поэтому фосфин (РН3) добывают
косвенными методами с фосфідів:
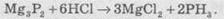
Фосфин
- это очень неустойчивое соединение, на воздухе он самовоспламеняется:
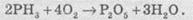
Фосфин
образуется при гниении на болотах и кладбищах, именно поэтому многие люди считают
процесс самовозгорания фосфина выходом души человека из тела.
Поскольку
белый фосфор может самовозгораться на воздухе, его остатки необходимо утилизировать,
для того чтобы избежать пожара. Отходы фосфора уничтожают с помощью раствора
купрум(ІІ) сульфата:
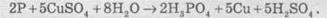
В
результате этой реакции кусочки белого фосфора покрываются металлической пленкой
меди и окисления фосфора становится невозможным.