МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА
2. СВОЙСТВА
ГАЗОВ (ГАЗОВЫЕ ЗАКОНЫ)
2.2. ГАЗОВЫЕ ЗАКОНЫ
2.2.2. ЗАКОН ГЕЙ-ЛЮССАКА (ИЗОБАРНЫЙ ПРОЦЕСС)
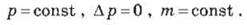
Изобарный процесс описывается законом
Гей-Люссака: для данной массы газа отношение объема и температуры является устойчивым, если
давление газа не меняется:
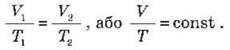
Закон Гей-Люссака можно подать в
виде
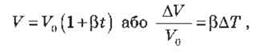
где t - температура по международной
шкале;
V0 - объем при 0 °С;
β - коэффициент объемного расширения
газа;
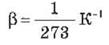 -
при постоянном давлении для идеального газа.
-
при постоянном давлении для идеального газа.
Ізобара - график зависимости между
параметрами состояния данной массы газа при постоянном давлении (рис. 6, 7).
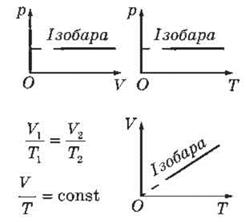
Рис. 6

Рис. 7