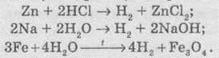ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ХИМИЯ ЭЛЕМЕНТОВ
ГИДРОГЕН.
ВОДОРОД. ВОДА
Водород
Характеристика химического элемента
Водород
- 1-й элемент Периодической системы (заряд ядра 1), химический знак - Н, относительная
атомная масса 1,008 (округленно 1). Валентность Водорода в соединениях равна
единицы, самый распространенный степень окисления +1. Молекула водорода Н2,
молекулярная масса 2,016 (округленно 2). Молярная масса 2 г/моль.
Распространенность
Водорода
Если
Кислород является самым распространенным элементом в земной коре, то Водород - самый распространенный
элемент во Вселенной. Водород составляет около 70% массы Солнца и звезд. Поскольку
Водород - самый легкий из всех элементов, то такая значительная масса требует огромного
количества атомов этого элемента. Из каждых 100 атомов, которые встречаются в
Вселенной, 90 - атомы Водорода.
Вероятно,
когда Водород входил в атмосферу Земли. Но из-за своей легкости он способен
покидать атмосферу, поэтому доля Водорода в воздухе чрезвычайно мала. В
связанном виде Водород составляет 0,76% массы Земли. Важнейшим соединением
Водорода, что случается в природе, есть вода.
Физические свойства
Водород
- газ, типичный неметал. Образует прочные ковалентные двухатомные молекулы Н2.
Нетрудно
подсчитать плотность водорода: 1 моль при обычных условиях занимает 22,4 л,
а молярная масса водорода равна 2 г. Следовательно, плотность в
пересчете на 1л составит 22 г/22,4 л = 0,09 г/л. Плотность воздуха
заметно выше - 1,305 г/л, поэтому наполненные водородом предметы испытывают выталкивающей
силы атмосферы.
Водород
становится жидким при очень низких температурах (-253 °С), а твердый водород добыть еще
тяжелее (температура плавления твердого водорода -259 °С).
Изотопы
Водорода
Атом
Водорода - самый простой из всех атомов. Его ядро состоит из единственного
протона. Этот (самый распространенный) изотоп Водорода называют также протієм, чтобы
отличить от дейтерия - другого изотопа Водорода, в ядре которого содержится 1
протон и 1 нейтрон. Дейтерий находится в природе в очень небольшом количестве.
Однако его научились выделять для нужд ядерной энергетики. Дейтерий - один из
немногих изотопов в химии, который имеет свой собственный символ D. Самой известной химическим соединением, к которой входит дейтерий, есть
«тяжелая вода» D2О.
В
ядерных реакциях образуется еще один изотоп Водорода - тритий, в ядре которого 1
протон и 2 нейтронов. Тритий (химический символ Т). радиоактивный и в природе не
случается.
Таким
образом, наиболее известны три изотопа Водорода: 11Н (или
просто Н), 12H (или D), 13Н
(или Т). В последнее время также добытые тяжелые изотопы Водорода с массой от 4 до
8.
Электронная
строение и положение
Водорода в Периодической системе
Поскольку
в ядре любого изотопа Водорода всегда только один протон, то электронная
оболочка включает только один электрон, занимающий нижний электронный уровень 1s. Таким образом, любой изотоп Водорода
имеет только одну - и к тому же валентную - оболочку 1s1.
Электронный
уровень 1s вмещает
не более 2-х электронов и атома Водорода достаточно присоединить или потерять один
электрон, чтобы достичь устойчивой электронной конфигурации:
Н
- 1ē
→
Н+ - положительный ион Водорода (в электронной оболочке отсутствуют
электроны)
Н
+ 1ē
→
H- - отрицательный ион Водорода (1s2)
Первое
уравнение свидетельствует о родственную связь Водорода с элементами группы -
щелочными металлами, которые охотно отдают единственный внешний электрон и образуют
положительные ионы Li+, Na+, К+ и т.д. Второе уравнение
свидетельствует о близости Водорода к элементам VII группы, которым не хватает
одного электрона для завершения внешней оболочки и которые легко принимают чужой
электрон с образованием ионов F-,
Сl-,
Вr-
т.д.
Типичными
неметаллическими свойствами этот элемент больше подобный элементов VII группы
(Фтора, Хлор, Бром и т.п.). Но Водород не является р-элементом и более охотно отдает
электрон, чем принимает. Поэтому его пребывание в группе s-элементов - активных восстановителей - также имеет смысл. В
связи с этим Водород часто помещают в И группу Периодической таблицы, а в VII
группе повторяют его символ в скобках. Но есть и такие издания Периодической таблицы, где его основным
местом является именно VII группа. И то и другое - правильно.
Методы
добыча
В
земных условиях Водород встречается преимущественно в связанном состоянии, в виде
соединений со степенью окисления +1.
Когда
Водород уже находится в степени окисления +1, он может отбирать электрон в
многих элементов, особенно металлов, которые склонны отдавать электроны. Поэтому
способы добывания водорода часто основываются на реакции какого-либо металла с
одним из соединений Водорода, например:
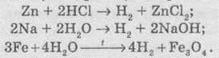
Реакцию
между цинком и водным раствором соляной кислоты чаще всего используют для
добыча водорода в лаборатории.
Вместо
цинка в реакции с НСl
можно использовать другие металлы (хотя и не любые) - например железо,
олово, магний.
А
реакция между железом и водяным паром при нагревании имеет историческое значение -
когда-то ее использовали для наполнения водородом воздушных шаров.
Движущей
силой подобных реакций добывания водорода является не только стремление отдать металлов
электрон атома Водорода в степени окисления +1, но и получить большую
количество энергии в случае скрепления нейтральных атомов Водорода, образующихся
при этом, в молекулу Н2. Поэтому в реакции такого типа вступают
даже неметаллы:

Эта
реакция лежит в основе промышленного способа добывания водорода. Водяной пар
пропускают над раскаленным до белого коксом (углем, который нагревается без
доступа воздуха). В результате образуется смесь карбон оксида с водородом, которую
называют «водяным газом».
Водород
может образоваться и вследствие сильного нагрева метана:
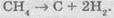
Поэтому
в промышленности большое количество водорода добывают именно из метана, добавляя к
него за высокой температуры перегретый водяной пар:
1) СН4 + Н2O = СО + 3Н2;
2) СО + Н2O = СO2 + Н2.
В
сумме этот процесс можно записать уравнением:
СН4
+ 2Н2O
= 4 Н2 + СO2.
Смесь
газов охлаждают и промывают водой под давлением. При этом СO2 растворяется, а
малорастворим в воде водород идет на промышленные нужды.
Чистейший
водород в промышленности получают электролизом воды:

Этот
способ требует больших затрат энергии, поэтому распространен меньше, чем
высокотемпературная реакция кокса или метана с водой. Существуют и другие способы
добывания водорода.
Химические
свойства Водорода
Водород
- один из рекордсменов по числу многообразие соединений. Наибольшее их количество
приходится на соединения с Карбоном, которые изучает органическая химия.
Но
и неорганические соединения Водорода очень разнообразны.
В
в таблице приведены примеры соединений Водорода с типичными s- и р-элементами,
Указанный степень окисления Водорода во всех соединениях.
|
Второй
период
|
|
литий гидрид
|
бериллий гидрид
|
метан
|
аммиак
|
вода
|
фтористый
водород
|
|
-1
|
-1
|
+1
|
+1
|
+1
|
+1
|
|
LiH
|
ВеH2
|
CH4
|
NH3
|
H2O
|
HF
|
|
твердый
|
твердый
|
газ
|
газ
|
жидкость
|
жидкость
|
|
Третий
период
|
|
магний гидрид
|
силан
|
фосфин
|
сероводород
|
хлористый
водород
|
|
-1
|
-1
|
-1
|
+1
|
+1
|
|
MgH2
|
SiH4
|
PH3
|
H2S
|
HCl
|
|
твердый
|
газ
|
газ
|
газ
|
газ
|
|
|
|
|
|
|
|
|
|
Соединения
металлов с Гідрогеном (они называются гидридами металлов) являются твердыми
веществами. Гидриды металлов можно добывать непосредственно из металла и водорода:
Са
+ Н2 → СаН2 (кальций гидрид, tпл = 1000 °С)
Гидриды
бурно реагируют с водой с образованием газуватого водорода:
СаН2
+ 2Н2O
→
Са(ОН)2 + 2Н2.
Это
еще один удобный способ добывания газуватого водорода. Источником атомов Водорода является
как гидрид металла, так и вода. Поэтому для добывания 1 м3 водорода
необходимо всего 0,94 кг
кальций гидрида, тогда как для получения того же количества газа действием металлов на
кислоты нужно 2,5 кг
железа или 2,9 кг
цинка.
Соединения
Водорода с неметаллами преимущественно являются газами. Исключение составляет вода и
фтороводорода. Такое резкое отличие воды от других летучих соединений Водорода
объясняется существованием между молекулами воды особого вида химической связи -
водородного.
С
всех соединений Водорода одной из важнейших является аммиак, который добывают реакцией
водорода с азотом при высокой температуре, давлении и в присутствии катализатора:

Это
один из немногих химических процессов, позволяющих связывать довольно инертный
атмосферный азот. В дальнейшем с более активного в химическом отношении аммиака
добывают множество нитратных соединений - нитратную кислоту, красители, взрывчатые
вещества, нитратные удобрения.
Восстановительные
свойства Водорода используют для получения чистых металлов из их
оксидов. Например, во время нагрева купрум(II) оксида СuО в струе водорода образуется вода и
порошок меди:
СuО + Н2 →
Сu + Н2O.
Для
некоторых очень тугоплавких металлов восстановления их оксидов водородом оказывается
удобным и экономичным способом добывания. Например, металл вольфрам, из которого
делают нити лампочек накаливания, добывают с помощью реакции:
WO3 + 3Н2
→
W + 3Н2O.
Металл
получается в виде порошка, который затем можно прессовать в готовые изделия. После
спекание такие изделия не требуют дальнейшей обработки. Этот способ добывания
металлов и деталей из них называется порошковой металлургией.
Применение
водорода
Водород
чрезвычайно теплотворним химическим топливом. Кроме того, в результате сжигания
водорода образуется только вода, тогда как другие топлива загрязняют атмосферу
оксидами Углерода, Азота и незгорілими остатками топлива.
Водород
используется в качестве горючего в современной ракетной технике. Ракетоносители способные
выводить на орбиту более 100 тонн различных грузов благодаря водородно-кислородным
двигателям. В их баках содержится жидкий кислород и жидкий водород.
Смеси
водорода с кислородом называются гремучим газом и взрываются от малейшей искры. Поэтому
работа с водородом как топливом требует таких мер предосторожности, которые бы исключали
возможность взрыва. Современная техника позволяет достичь высокого уровня безопасности, но
история знает трагедии, связанные со взрывами водорода.
В
первой половине века в разных странах было построено большое количество
летательных аппаратов, легких воздуха - дирижаблей.
Дирижабли
- это управляемые аэростаты со сигароподібною оболочкой, наполненной водородом. Большой
объем водорода в оболочке обеспечивал высокую грузоподъемность этих воздушных кораблей.
Крупнейшие пассажирские дирижабли 30-х годов XX века могли перевозить до 100
человек на очень большие расстояния. На этих летательных аппаратах были комфортабельные
каюты, рестораны, душевые, палубы для прогулок и т.д. Такие дирижабли
осуществляли регулярные рейсы из Европы в Америку.
Однако
большое количество энергии, выделяющейся в реакции водорода с кислородом, таит в себе
огромную опасность. 6 мая 1937 года крупнейший в мире пассажирский
дирижабль «Гинденбург», который прилетел из Германии в Нью-Джерси (США), взорвался и
упал на землю от искры, которая проскочила между причальною мачтой и корпусом дирижабля.
Во многом именно через эту катастрофу строительство пассажирских дирижаблей
вскоре прекратилось.
В
наше время водород не применяют для наполнения аэростатов и других летательных
аппаратов, легких воздуха. Для этих целей используют более дорогой, и
однако безопасный газ гелий.