|
Луга
|
Нерастворимые
гидроксиды
|
|
Изменяют окраску индикаторов
|
|
|
Взаимодействуют с кислотами с образованием
соли и воды (реакция нейтрализации):
2KOH + H2SO4
→ K2SO4
+ 2Н2O
|
Взаимодействуют с кислотами с образованием
соли и воды (реакция нейтрализации):
Fe(OH)2 +
H2SO4 →
FeSO4 +
2Н2O
|
|
Взаимодействуют с кислотными оксидами:
2NaOH +
СO2
→
Na2CO3 +
Н2O
|
Взаимодействуют с кислотными оксидами
(ангидридами сильных кислот):
2Fe(OH)3 +
3SO3 → Fe2 (SO4)3 + 3H2O
|
|
Взаимодействуют с амфотерными оксидами и
гидроксидами:
2NaOH + ZnO → Na2ZnO2 + Н2O;
KOH + Al(OH)3 →
KAl(OH)4
|
|
|
Взаимодействуют с солями, если
выполняется хотя бы одно условие протекания реакций обмена:
2NaOH + CuSO4 → Сu(ОН)2 ↓ + Na2SO4;
NaOH +
NaHCO3 → Na2CO3 + CO2 ↑ + H2O
|
|
|
Гидроксиды щелочных металлов устойчивы к
нагрев, гидроксиды щелочноземельных металлов разлагаются, но при более
высокой температуре, чем нерастворимые гидроксиды:
Са(ОН)2 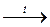 СаO + Н2O СаO + Н2O
|
При нагревании разлагаются:
2Fe(OH)3 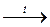 Fe2O3
+ 3H2O Fe2O3
+ 3H2O
|