|
Тема. Строение атома
Цель урока: рассказать ученикам о строении атома; ознакомить их с планетарной моделью атома по Резерфордом. Тип урока: урок изучения нового материала. ПЛАН УРОКА
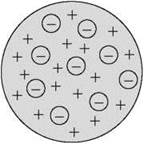
ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА К 1902 г. было осуществлено достаточно экспериментов, которые убедительно доказали, что электрон является одной из основных составных частей любого вещества. Джозеф Джон Томсон показал на основе классической электромагнитной теории, что размеры электрона должны быть около 10-15 м. Кроме того, было известно, что размеры атомов составляют несколько ангстрем (один ангстрем равен 10-10 м). На этом основании Томсон 1903 г. предложил модель атома, согласно которой атомы представляют собой однородные шары из положительно заряженного вещества, в котором находятся электроны. Суммарный заряд электронов равен положительному заряду атома. Поэтому атом в целом электрически нейтрален. Эта модель получила название «пудинг», потому что электроны были вкраплены в положительно заряженное среду подобно изюму в пудинге.
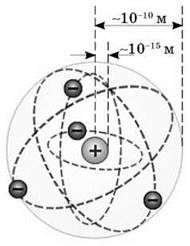
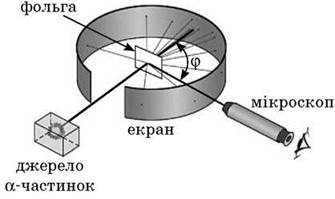
Отклонение электрона в атоме от положения равновесия приводит к возникновению вращательной силы. Поэтому электрон, выведенный в определенный способ из положения равновесия, совершает колебания, а потому является источником электромагнитного излучения. Модель Томсона казалась привлекательной с точки зрения того, что предполагала наличие электронов в атоме. Однако она просуществовала только до 1911 года. Резерфорд предложил своим сотрудникам экспериментально проверить состоятельность модели атома Томсона. Идея опыта была проста. Если модель атома Томсона соответствует действительности, то, пропуская через очень тонкую металлическую пленку узкий пучок быстрых α-частиц, экспериментаторы не должны обнаружить сколько-нибудь заметного отклонения этих частиц. Резерфорд установил, что каждая α-частица, попадая на экран из сернистого цинка, вызывает вспышку света. Рассеявшись в золотой фольге, α-частицы попадали затем на экран, и их потом регистрировал микроскоп. Стоило надеяться, что пучок α-частиц при прохождении через тонкую фольгу слегка расплывется на незначительные углы. Такое рассеяние на малые углы действительно наблюдалось, но совершенно неожиданно оказалось, что примерно одна α-частица из 20 000, что падают на золотую фольгу толщиной всего лишь 4·10-5 см, возвращается обратно, в сторону источника. Резерфорду понадобилось несколько лет, чтобы окончательно понять столь неожиданное рассеяния α-частиц на большие углы. Он пришел к выводу, что положительный заряд атома сосредоточен в очень малом объеме в центре атома, а не распределен по всему атоме, как в модели Томсона. Резерфорд сумел определить размер атомного ядра. И оказалось, что атомное ядро в десятки тысяч раз меньше собственно атом: размер ядра - порядка 10-14-10-15 м, в то время как размер атома - около 10-10 метров. Основываясь на своих опытах и расчетах, Резерфорд предложил планетарную модель атома: · атомы любого элемента состоят из положительно заряженной части, получившей название ядра; · в состав ядра входят положительно заряженные элементарные частицы - протоны (позже было установлено, что и нейтральные нейтроны); · вокруг ядра вращаются электроны, образующие так называемую электронную оболочку. Подобие атома до Солнечной системы усиливалось тем, что закон Кулона, что «управляет» движением электронов, совпадает по форме с законом всемирного тяготения, что «управляет» движением планет: и в том, и в другом случае сила обратно пропорциональна квадрату расстояния. 4. Недостатки планетарной модели атома Несмотря на всю убедительность планетарной модели возникал целый ряд непреодолимых трудностей во время объяснения строения атома. Согласно классической теории, система, состоящая из массивного положительно заряженного ядра и легких, отрицательно заряженных электронов, может быть устойчивой только в том случае, когда электроны находятся в движении. Таким образом, атом должен быть подобен миниатюрной Солнечной системе, в которой роль Солнца играет ядро, а планет - электрон. Аналогия была бы полной (ведь электрические и гравитационные силы зависят от расстояния как 1/r2), если бы не одно предсказания классической теории, согласно которому электрические заряды, ускоренно движутся, должны излучать энергию в виде электромагнитных волн. Поэтому электроны, двигаясь по «планетарных» орбитах, должны были бы во время излучения терять энергию движения и в результате быстро приближаться к ядру. Расчеты показывали, что электрон в атоме Водорода имеет излучать всю свою энергию за малую долю секунды. Однако в атоме этого не происходит.
С другой стороны, если бы электроны двигались вокруг ядра подобно планетам вокруг Солнца, то каждый атом был бы единственным в своем роде, потому что, согласно классической механике, каждый электрон мог бы двигаться по каждой из бесконечного количества орбит. И поэтому должна была бы наблюдаться бесконечное разнообразие атомов одного и того же химического элемента. Таким образом, в «атомных масштабах» противоречит опыту не только классическая электродинамика, но и классическая механика - основа основ всей классической физики. ВОПРОС К УЧАЩИМСЯ В ХОДЕ ИЗЛОЖЕНИЯ НОВОГО МАТЕРИАЛА Первый уровень 1. Почему отрицательно заряженные частицы атома не имеют заметного влияния на рассеяние α-частиц? 2. Почему а-частицы не могли бы рассеиваться на большие углы, если положительный заряд атома был распределен по всему его объему? 3. Какие частицы входят в состав ядра? 4. Чем отличаются друг от друга атомы различных химических элементов? Второй уровень 1. На основании экспериментальных данных Резерфорд сформулировал планетарную модель атома? 2. Почему планетарная модель атома не согласуется с законами классической физики? 3. Что является главной характеристикой определенного химического элемента?
ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО МАТЕРИАЛА 1). Качественные вопросы 1. Во что превращается атом Натрия, если из его ядра «забрать» один протон, не изменяя количества электронов? 2. Сколько протонов, нейтронов и электронов в положительном ионе Лития? 2). Учимся решать задачи 1. В ядре атома Углерода содержится 12 частиц. Вокруг ядра движутся 6 электронов. Сколько в ядре этого атома протонов и нейтронов? 2. Будет ли меняться количество α-частиц, рассеянных под определенным углом, если в опыте Резерфорда увеличить толщину фольги вдвое?
Схема опыта Резерфорда ЧТО МЫ УЗНАЛИ НА УРОКЕ Планетарная модель атома: · атомы любого элемента состоят из положительно заряженной части, получившей название ядра; · в состав ядра входят положительно заряженные элементарные частицы - протоны (позже было установлено, что и нейтральные нейтроны); · вокруг ядра вращаются электроны, образующие так называемую электронную оболочку. Домашнее задание Подр.: § 27 (п. 1).
|
|