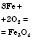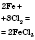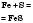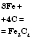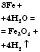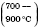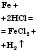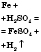Ферум. Оксиды и гидроксиды Железа
Ферум
Элемент
Феррум расположен в VIIIБ группе (VIII группе, побочной подгруппе), в 4 периоде.
Электронная конфигурация атома Железа:
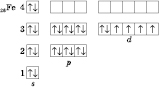
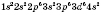
Валентными у Железа есть электроны как последнего, так и предпоследнего уровня
d-подуровня. Наиболее характерные степени окисления в соединениях +2 и +3.
Феррум - второй по распространенности в природе металл (после Алюминия). Важнейшие железные руды: магнитный железняк, красный железняк, бурый железняк, пирит.
Физические свойства.
Белый серебристый металл, плотность 7,87 г/см
3,
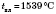
. Пластичный, тепло - и электрически ведущий, легко намагничивается и размагничивается.
Добывания.
Восстановление карбон(II) оксидом, алюмінотермія (см. производство чугуна и стали).
Химические свойства.
Металл средней активности (см. таблицу).
Химические свойства Железа
| Реагент | Уравнение реакции | Продукты реакции | Условия протекания реакции |
| Кислород | 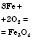 | Железная окалина (ферум(ІІ, ІІІ) оксид) | Горения в кислороде |
| Хлор | 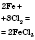 | Ферум(III) хлорид | Нагрев |
| Сера | 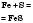 | Феррум(II) сульфид | Нагрев |
| Уголь (углерод) | 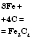 | Ферум карбид (цементит) | Высокая температура |
| Вода | 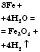 | Железная окалина и водород | Высокая температура 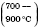 |
| Хлоридная кислота | 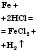 | Феррум(II) хлорид | Обычные условия |
| Разбавленная сульфатная кислота * | 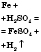 | Феррум(II) сульфат | Обычные условия |
| Растворы солей менее активных металлов | 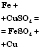 | Феррум(II) сульфат и медь | Обычные условия |
* Концентрированные сульфатная и азотная кислоты на холоде пассивируют железо.
Применение:
- катализатор;
- машиностроение;
- добывание сплавов - чугуна и стали.
Феррум(ii) оксид FeO
Черный порошок, который легко окисляется. В воде практически нерастворим.
Добыча:
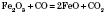
Химические свойства. Основной оксид, характерна взаимодействие с кислотами:
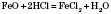
.
Феррум(iii) оксид
Самая стойкая естественная оксигеновмісна соединение Железа. В воде практически нерастворим.
Добывания. Разложение ферум(III) гидроксида при нагревании:
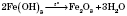
Химические свойства. Слабо амфотерный оксид.
Феррум(ii) гидроксид
Осадок белого цвета. На воздухе окисляется до ферум(III) гидроксида, окраска становится зеленоватым, а затем бурым:
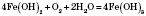
Добывания. Действие растворов щелочей на растворы солей железа(II):
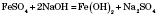
Химические свойства. Слабый амфотерный гидроксид. Характерна взаимодействие с кислотами:
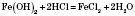
Феррум(iii) гидроксид
Осадок красно-бурого цвета.
Добывания. Действие растворов щелочей на растворы солей железа(III):
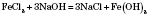
Химические свойства. Основной гидроксид. Характерна взаимодействие с кислотами:
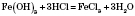
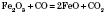
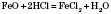 .
.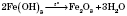
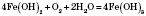
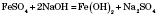
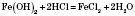
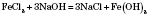
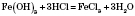

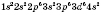
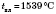 . Пластичный, тепло - и электрически ведущий, легко намагничивается и размагничивается.
. Пластичный, тепло - и электрически ведущий, легко намагничивается и размагничивается.